多囊卵巢综合征(专业版)
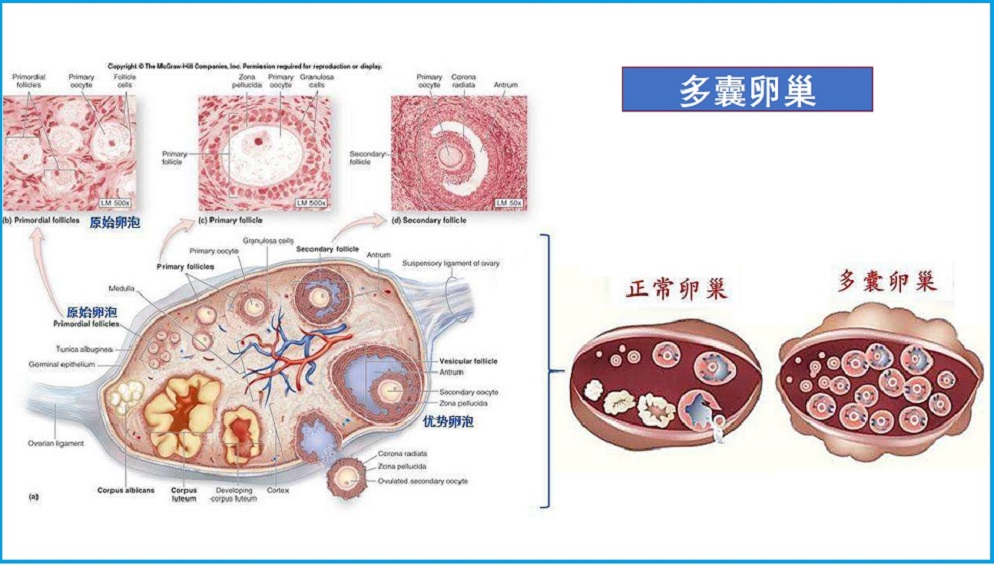
多囊卵巢综合征(PCOS)是一种常见的、最复杂的慢性内分泌疾病。卵巢生成卵泡,但卵泡不成熟、无法每月正常释放一个成熟的卵子。
其他名称:多滤泡卵巢现象;多囊卵巢病
英文名称:Polycystic Ovary Syndrome, PCOS;Polyfollicular Ovarian Appearance
在有症状的女性中,PCOS可能引起如下:
调整饮食与生活方式
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控多囊卵巢综合征的营养和草本补充剂,主要包括如下:
1.肌醇:
肌醇(Inositol)是一种存在于植物中的糖醇(纤维糖),并可在人体内产生,具有多种结构形式或异构体。其中,和肌醇(Myo-inositol)是自然界中分布最广泛的异构体,在卵巢中含量丰富。D-手性肌醇(DCI)异构体在体内的含量较少,有些和肌醇在体内转化为DCI1,2。
肌醇异构体以游离形式存在于细胞中,并作为膜磷脂的成分,在细胞间信号传导中具有活性1。此外,肌醇磷酸盐充当多种激素的第二信使,包括胰岛素和FSH,通过将外部信号传输到细胞的工作内部2-4。肌醇磷酸系统的失调与胰岛素抵抗和相关疾病有关,包括多囊卵巢综合征(PCOS)4,5。在临床试验中,和肌醇及DCI都对葡萄糖调节有积极作用;然而,和肌醇和DCI似乎对卵巢和垂体激素的产生有不同的影响,和肌醇与DCI治疗PCOS的最佳比例仍未确定3。
1.1.和肌醇(Myo-inositol,通称肌醇):
许多临床试验已经证明,和肌醇可以改善胰岛素敏感性和代谢标志物,也会影响PCOS女性的卵巢功能2,6,7。一项对6项随机对照试验(含355名参与者)的荟萃分析发现,与二甲双胍相比,和肌醇在对空腹胰岛素和胰岛素敏感性、睾酮、PCOS患者的性激素结合球蛋白(SHBG)和体重指数(BMI)的作用相当,而二甲双胍治疗的不良反应风险更高8。
补充和肌醇也被证明可以提高生育能力。一项随机对照试验对120名接受促排卵的PCOS相关的不孕妇女进行了为期三个月的每日二甲双胍加1800mg肌醇与单独二甲双胍的比较。与单独使用二甲双胍治疗的妇女相比,接受二甲双胍和肌醇治疗的妇女的成功分娩率增加了一倍多(分别为55%和27%)9。另一项针对116名PCOS相关不孕症妇女的随机对照试验发现,与同时接受肌醇和二甲双胍治疗的妇女相比,每天接受4g肌醇治疗6个月的女性在代谢标志物和激素水平方面有相当的改善。与单独使用肌醇相比,添加二甲双胍对受孕没有显著优势。二甲双胍组的副作用更多,主要是胃肠道副作用10。其他研究表明,在多囊卵巢综合征患者不孕治疗期间,补充肌醇可降低卵巢过度刺激综合征的风险7,11。
1.2. D-手性肌醇(DCI):
D-手性肌醇对介导胰岛素反应很重要,已被证明可以改善PCOS患者的胰岛素敏感性和改善与胰岛素抵抗相关的代谢状况12。通过恢复胰岛素活性,DCI补充剂可能有助于改善卵巢功能。然而,DCI也被发现可以抑制芳香化酶(一种促进卵巢中雄激素转化为雌激素的酶),并且发现更高剂量的DCI可以增加PCOS女性的循环睾酮水平3,13。此外,高剂量DCI可能会干扰肌醇的吸收,从而降低治疗效果的可能性,尽管目前还没有关于这种关系的结论性数据3。
1.3.和肌醇加D-手性肌醇:
由于二者的作用不同,和肌醇和DCI可能具有互补作用。建议将肌醇与DCI的比例定为40:1,因为这被认为反映了血浆中这些化合物的生理平衡3,14。一项针对56名PCOS患者的随机对照试验将使用七种不同配方的每天4g肌醇与单独DCI或肌醇与DCI的效果进行了比较,其比例如下:1:3.5、2.5:1、5:1、20:1、40:1,或80:1。和肌醇与DCI的比例为40:1,对恢复排卵和一系列生殖激素的正常水平最为有效,而所有配方都能改善代谢标志物14。
一项针对46名PCOS和肥胖参与者的随机对照试验,比较了六个月的和肌醇加DCI联合每日治疗的效果,其比例为40:1(含1100mg肌醇)加400mcg叶酸与每天400mcg单独叶酸。接受肌醇加DCI治疗的患者LH、游离睾酮和空腹胰岛素水平降低幅度更大,雌激素水平升高,胰岛素敏感性改善15。在另一项对44名超重或肥胖PCOS患者的对照试验中,10名患者接受饮食、4g肌醇和400mcg叶酸的治疗;13名以40:1的比例加入肌醇和DCI(含1,100mg肌醇);单独饮食组21名。在所有组中体重、BMI、臀围和腰围都显著下降,而只有比例为40:1的组月经规律得到了显著恢复16。
在一项对照试验中,对11名患有PCOS相关不孕并接受体外受精(IVF)的女性在接受550mg肌醇加每天300mg或27.6mg DCI治疗12周后获得的卵母细胞质量进行了评估。研究发现,更高剂量的DCI对卵母细胞质量有更大的积极影响17。
2. N-乙酰半胱氨酸(NAC):
已知NAC是含硫氨基酸半胱氨酸的一种形式,也是谷胱甘肽的前体,谷胱甘肽是人体内最重要的抗氧化剂和解毒剂之一。
一项针对100名PCOS受试者的随机对照试验将NAC(1800mg/天)和二甲双胍(1500mg/天)治疗24周进行了比较。NAC治疗显著改善了BMI、腰围和腰臀比,而二甲双胍则没有。此外,NAC显著改善了胰岛素敏感性标志物,如空腹胰岛素、空腹血糖和空腹血糖/胰岛素比值,但二甲双胍没有改善。NAC治疗的参与者的总睾酮水平下降幅度更大,副作用更少18。
多项对照试验表明,NAC可以提高促排卵药物对多囊卵巢综合征不孕妇女的疗效。在一项随机对照试验中,162名接受生育药物柠檬酸克罗米芬(Clomid)治疗失败的PCOS相关不孕症妇女比较了在治疗中添加NAC或L肉碱三个月的效果。NAC组在游离睾酮水平和胰岛素抵抗标志物方面有更大的改善,而两组在月经规律、LH和FSH水平方面都有类似的改善;然而,只有L-肉碱组的血脂水平有所改善19。在另一项对照试验中,将每天1800mg NAC与1500mg二甲双胍作为克罗米芬柠檬酸盐治疗的补充,对108名克罗米芬耐药PCOS相关不孕妇女进行了比较。NAC导致不想要的头发生长和空腹血糖水平的大幅下降;二甲双胍使BMI和胰岛素水平显著降低。此外,NAC和二甲双胍对12周后的排卵率和生育率也有类似的积极作用20。
NAC也可能有助于接受来曲唑(Femara)不孕治疗的妇女。一项针对130名PCOS患者的双盲、随机、安慰剂对照试验显示,与单独使用来曲唑或安慰剂相比,来曲唑联合每天1200mg NAC可在5天后产生更多直径大于18mm(与排卵可能性较大相关)的卵泡。此外,接受NAC作为来曲唑辅助治疗的患者排卵率和妊娠率较高21。然而,另一项包括97名PCOS患者的随机对照试验发现,每天1200mg NAC并不能改善克罗米芬和来曲唑联合治疗的促排卵效果22。
NAC作为试管婴儿之前的支持性治疗也可能有价值。在一项对80名准备试管婴儿的PCOS妇女进行的安慰剂对照试验中,每天1800mg NAC持续六周似乎可以改善卵细胞的质量23。
3. 维生素D:
维生素D在生殖和代谢健康中的重要作用越来越受到人们的认可,维生素D缺乏可能会导致PCOS女性的激素、代谢和心理健康障碍24-26。一项观察性研究发现,维生素D不足与PCOS女性较高的雄性激素水平和BMI有关,另一项研究发现,维生素D缺乏症在患有PCOS的女性中比没有PCOS的女性更常见27,28。
多项随机对照试验和荟萃分析表明,维生素D治疗对PCOS妇女的代谢和激素健康有有益影响。一项荟萃分析包括了11项随机对照试验的数据,这些试验共涉及483名PCOS女性。该荟萃分析发现,维生素D的剂量范围为每天4000–7143IUs(100–179mcg),可降低总睾酮、胰岛素抵抗、总胆固醇和LDL胆固醇29。对许多相同试验的其他荟萃分析也得出了类似的结论,发现维生素D对PCOS女性,特别是维生素D缺乏症女性的脂质代谢和葡萄糖代谢有广泛的积极影响。
在一项为期12周的随机安慰剂对照试验中,30名患有PCOS和维生素D缺乏症的超重女性(18-49岁)每周服用50,000IU(1250 mcg)维生素D,补充维生素D可减少多余的头发生长和雄性激素水平30,31。在另一项随机对照试验中包括180名患有PCOS的女性和150名未患有PCOS女性,所有患者的血清25-OH维生素D水平均低于30ng/mL,而那些每周接受20,000 IU(500mcg)维生素D的PCOS患者的LH:FSH比率与安慰剂相比有所改善32。
4. 欧米伽3脂肪酸:
ω-3脂肪酸的抗炎活性可以减少PCOS的心血管、代谢和激素并发症33。一项针对325名PCOS女性和325名健康对照的病例对照研究发现,PCOS女性血清磷脂中的ω-3脂肪含量较低。ω-3含量最高的三分之一的女性患多囊卵巢综合征的几率比含量最低的三分之一的女性低30-40%34。
一项包括9项随机对照试验的统计分析,共涉及591名PCOS女性,还报告发现补充ω-3脂肪酸可以改善胰岛素敏感性,降低总胆固醇和甘油三酯水平,以及脂联素(一种主要由脂肪组织产生的信号肽,可提高胰岛素敏感性并具有抗炎特性)水平35,36。另一项统计分析发现,补充Omega-3脂肪酸可降低PCOS女性的高敏C反应蛋白(hs-CRP)水平,增加脂联素水平37。
在一项针对88名PCOS女性的随机对照试验中,连续六个月每天补充2000mg鱼油中的ω-3脂肪酸(包括360mg EPA和240mg DHA),可降低腰围、甘油三酯和胆固醇水平38。
5. 镁:
镁在调节葡萄糖代谢和胰岛素敏感性方面起着重要作用,低镁状态可能是胰岛素抵抗发展为2型糖尿病和心脏病的一个促成因素39。对总共2000多名女性的8项研究进行的统计分析发现,患有PCOS的超重或肥胖女性的血清镁浓度低于患有PCOS的正常体重女性40。此外,一项对1000多名PCOS患者的镁状况进行调查的研究发现,镁水平越低,胰岛素抵抗越差,睾酮水平越高41。
另一项针对60名PCOS患者的安慰剂对照试验发现,连续8周每天250mg氧化镁可增加LH水平并降低BMI,但不会影响葡萄糖或脂质代谢标志物或多种激素状态指数42。
6. 硫辛酸:
硫辛酸(ALA)是一种重要的抗氧化营养素,已被证明可支持健康的葡萄糖代谢43。一项大型统计分析发现,ALA可降低血清胰岛素并提高胰岛素敏感性44。在一项针对32名PCOS和肥胖女性的非对照试验中,每天400mg ALA治疗12周可降低胰岛素和葡萄糖水平、BMI和胰岛素抵抗45。在另一项小型非对照试验中,6名患有PCOS的正常体重女性服用600mg控释硫辛酸,每天两次,持续16周。胰岛素抵抗、甘油三酯水平和低密度脂蛋白颗粒大小得到改善。此外,未服用口服避孕药的两名受试者的月经不规律也有所改善46。
几项临床试验已经注意到硫辛酸和肌醇的组合对PCOS的生物标志物和症状的积极影响。在一项针对23名PCOS青少年和21名健康对照的病例对照研究中,研究了肌醇加硫辛酸治疗6个月。治疗显著降低了胰岛素抵抗和血清胰岛素水平47。在一项针对40名PCOS女性的非对照试点研究中,肌醇和硫辛酸的组合降低了雄性激素水平,改善了月经规律,在不影响葡萄糖或胰岛素参数的情况下,减少了多余的头发生长和BMI48。在一项对44名月经不频繁的PCOS患者进行的非对照试验中,每天800mg硫辛酸和2000mg肌醇进行24个月的长期治疗,显著减少了月经不规律49。在一项针对71名PCOS女性的为期六个月的非对照试验中,每天800mg ALA加1000或2000mg肌醇改善了月经规律。然而,从中受益的1000mg的女性要少得多50。
7.铬:
矿物铬由于其支持葡萄糖调节和代谢健康的能力,可能对PCOS妇女有益51。一项针对42名PCOS妇女(14名患有代谢综合征,28名未患有)的病例对照研究发现,代谢综合征和PCOS的参与者铬和几种抗氧化微量营养素的摄入量较低52。
在一项双盲、随机、对照试验中,85名患有PCOS女性在六个月内每天接受1000mcg吡啶甲酸铬或安慰剂治疗,补充吡啶甲酸铬可显著改善BMI和空腹血清胰岛素水平。补充铬也使五个月后排卵和月经规律的机会增加了近两倍53。在一项小型试点试验中,该试验招募了10名PCOS女性,并将她们随机分组,每天接受200mcg吡啶甲酸铬或安慰剂治疗,为期四个月,补充铬改善了葡萄糖耐量,但没有改善排卵频率54。另一项小型研究也报道了患有PCOS的肥胖女性补充1000mcg吡啶甲酸铬后葡萄糖代谢的改善55。
对七项随机对照试验数据的统计分析发现,补充铬显著降低了BMI和游离睾酮水平56。然而,另一项荟萃分析包括6项随机对照试验,共有351名参与者,发现尽管补充铬降低了胰岛素抵抗,但也显著提高了总睾酮和游离睾酮水平57。基于这些关于游离睾酮水平的荟萃分析得出的不同结论,对于选择服用铬的PCOS女性来说,定期监测她们的游离睾酮水平是谨慎的。
8. L-肉碱:
L-肉碱是一种在脂质代谢中起关键作用的氨基酸。临床证据表明,它可能有助于治疗代谢紊乱,如2型糖尿病和非酒精性脂肪肝(NAFLD)58,59。一项观察性研究发现,患有PCOS的女性,尤其是肥胖女性,其L-肉碱水平低于无PCOS的女性60。
在一项针对74名PCOS妇女的非对照试验中,在三个月的时间里,每天服用3g L-肉碱可显著改善胰岛素敏感性、BMI、多余的头发生长、脂质水平和月经周期规律61。一项随机对照试验纳入了170名PCOS相关不孕妇女,她们已被证明对克罗米芬的作用具有耐药性。参与者被随机分配在月经周期的第3-7天接受150mg克罗米芬、安慰剂或3g L-肉碱的治疗。与安慰剂相比,L肉碱提高了排卵率(64.4%对17.4%)和妊娠率(51.5%对5.8%)62。
在一项针对147名PCOS女性的随机安慰剂对照试验中,发现乙酰L肉碱(ALC)形式的L肉碱,剂量为500mg,每日两次,可增加抗糖尿病药物二甲双胍和吡格列酮(Actos)的益处。一组只接受药物治疗,另一组接受药物加ALC治疗,第三组接受安慰剂治疗。两种积极治疗都导致血清胰岛素水平下降,尽管在接受ALC的组中效果更为明显。促黄体生成素(LH)降低,心理评分提高,也以类似的方式。两种治疗都能提高血清脂联素和胰岛素敏感性,并提高睾酮和FSH水平。只有接受ALC治疗的患者月经规律和腰围才有所改善63。
9.益生菌:
肠道微生物组在调节免疫功能和代谢方面发挥着关键作用,并可能在PCOS中不必要的毛发生长中发挥作用64。对17项随机对照试验的统计分析发现,摄入益生菌、益生元或合生元(益生菌加益生元)对PCOS的代谢方面有益。具体而言,空腹血糖和胰岛素水平、胰岛素敏感性、总胆固醇和LDL胆固醇以及甘油三酯水平均有改善65。另一项对共有587名参与者的9项随机对照试验结果的统计分析发现,使用益生菌或合生元治疗8周或更长时间,可以改善多余的头发生长、空腹血糖和胰岛素、胰岛素敏感性和BMI。此外,睾酮以及炎症和氧化应激指标也有所改善66。
然而,在一项针对99名PCOS患者的安慰剂对照试验中,提供益生元菊粉的合生元补充剂加上七种益生菌菌株的组合治疗12周,可以改善LDL和HDL胆固醇水平,但没有改变甘油三酯水平、体重或身体成分67。
10.黄连素:
黄连素(又称小檗碱)是一种生物活性生物碱,存在于包括伏牛、白毛茛等几种药用植物中68。这些植物已被广泛用于亚洲传统医学中治疗感染、代谢紊乱和其他适应症。黄连素在改善胰岛素敏感性、降低血清雄激素和调节慢性炎症方面的疗效使其成为多囊卵巢综合征研究的一个主题69-72。91-94
一项针对89名患有PCOS和胰岛素抵抗的女性的试验发现,与二甲双胍或安慰剂以及相同激素治疗的组合相比,黄连素与激素治疗相结合,可以改善脂质状况和SHBG水平,以及糖代谢和腰围73。在一项小型临床试验中,12名新诊断为PCOS妇女服用550mg黄连素磷脂复合物,每天两次,持续60天。治疗后,胰岛素敏感性、睾酮水平和炎症标志物显著改善69。黄连素也可能改善体外受精结果:150名接受体外受精治疗的PCOS妇女在卵巢刺激前随机接受二甲双胍、黄连素或安慰剂治疗三个月。与安慰剂组相比,服用二甲双胍或黄连素的女性睾酮和胰岛素抵抗降低,妊娠率增加。与二甲双胍相比,服用黄连素的妇女活产率也有所提高,不良反应更少74。
黄连素被认为通过抑制PI3K/AKT和MAPK途径、激活AMPK以及与多种其他靶点相互作用来影响激素水平和胰岛素代谢72,75。此外,黄连素可以通过降低几种促炎标志物的水平来改善PCOS病理的某些方面,如核因子κB(NF-κB)、肿瘤坏死因子α,以及白细胞介素1(IL-1)和6(IL-6)76。
尽管在人体临床试验中对黄连素进行了研究,并证明其具有多种代谢益处,但在某些临床前研究的基础上,人们对长期使用黄连素表示担忧77-79。一些证据表明,长期使用黄连素,尤其是高剂量的黄连素,可能会损害特定类型细胞中细胞代谢的某些方面。这项临床前研究的意义尚待长期人体临床试验确定。因此,目前建议短期使用黄连素为宜。
11.肉桂:
对多项临床试验的一项综述得出结论,,每天1-6g肉桂树皮粉末,对2型糖尿病患者具有降血糖作用80。肉桂在临床和临床前环境中都表现出抗高血压、抗肥胖和降脂的特性,使其可能成为代谢综合征和PCOS治疗的候选药物81,82。
对五项随机对照试验的统计分析发现,肉桂可以改善PCOS女性的胰岛素抵抗83。在其中一项试验中,80名PCOS女性被随机分配接受每天1.5g肉桂粉,分三次服用,或安慰剂治疗12周。肉桂组在空腹胰岛素、胰岛素抵抗和LDL胆固醇方面的下降幅度明显大于安慰剂组84。在一项针对84名患有PCOS和超重或肥胖的受试者(20-38岁)的安慰剂对照试验中,8周内每天1.5g肉桂可提高抗氧化状态,减少氧化应激,改善总胆固醇、LDL和HDL胆固醇水平85。在PCOS的啮齿动物模型中,在雄激素治疗中添加肉桂会减弱单独雄激素治疗时卵巢功能和结构的变化;肉桂的添加也导致了更正常水平的多种性激素86。
12.姜黄素:
姜黄素可减少氧化应激和炎症,并已被证明可改善葡萄糖和脂质代谢以及胰岛素敏感性87。对三项随机对照试验的统计分析发现,每天补充500–1500mg的姜黄素可改善空腹血糖,PCOS患者的胰岛素水平、胰岛素敏感性以及高密度脂蛋白和总胆固醇88。
在荟萃分析中的一项试验中,60名PCOS患者接受了500mg姜黄素或安慰剂治疗,每天两次,为期六周。与安慰剂相比,姜黄素治疗的PCOS女性血清胰岛素显著降低,胰岛素敏感性改善89。在统计分析的另一项试验中,67名PCOS女性接受了500mg姜黄素,每日三次或安慰剂治疗,持续12周。试验结束时,与对照组相比,姜黄素组的空腹血糖和雄激素水平显著下降90。在一项针对72名PCOS患者的对照试验中,每天服用1500mg姜黄素治疗12周,也显示出比安慰剂更能上调PPAR-γ激活分子的表达,改善氧化应激标志物91。
13.白藜芦醇:
白藜芦醇是一种存在于葡萄皮、花生和日本虎杖等抗氧化、抗炎的植物多酚,并在动物研究和临床试验中都证明了其雌激素作用92,93。动物和人类研究的结果表明,白藜芦醇可改善PCOS的代谢参数、雄激素水平、卵巢功能和生育能力94。
在78名多囊卵巢综合征患者的随机安慰剂对照试验中,每天服用1000mg白藜芦醇三个月后,月经规律增加,脱发减少,但其他生殖和代谢指标没有变化95。一项针对30名多囊卵巢综合征(PCOS)女性的随机对照试验发现,连续三个月每天1,500mg白藜芦醇可降低总睾酮、硫酸脱氢表雄酮(DHEA-S)和空腹胰岛素水平;白藜芦醇治疗也增加了胰岛素敏感性96。
在一项随机对照试验中,61名PCOS相关不孕妇女在诱导排卵和取卵进行试管婴儿之前,每天服用800mg白藜芦醇或安慰剂40天。那些接受白藜芦醇治疗的患者有更多高质量的卵母细胞和受精后胚胎。与安慰剂相比,还发现降低了总睾酮和LH水平,增加了FSH水平97。一项针对40名PCOS患者的公开试验发现,每天服用40天800mg白藜芦醇,可以降低炎症细胞因子和CRP水平,以及一种称为内质网应激的细胞应激标志物水平98。内质网应激引起的异常蛋白被认为在PCOS相关的卵巢功能障碍中发挥作用99。
14.褪黑素:
褪黑素是由松果体分泌的一种激素,调节体内的睡眠-觉醒(昼夜节律)周期,并具有清除自由基的作用。在健康个体中,褪黑素水平呈现出每日规律,在晚上达到峰值,在早上下降。褪黑激素受体的遗传变异与PCOS的风险增加有关,睡眠障碍包括睡眠呼吸暂停在PCOS患者中很常见100。
PCOS患者的昼夜节律控制系统似乎失调。在一项包括321名有或没有PCOS症状的女性志愿者的研究中,较高的早晨褪黑激素水平与较多的PCOS相关特征(雄激素过多、少或无月经、卵巢囊性)的表达相关,这表明PCOS可能与昼夜节律信号中断有关。该研究还发现,早晨皮质醇水平过高与PCOS症状数量之间存在关系。由于皮质醇分泌也遵循与褪黑激素大致相反的昼夜节律模式,这一发现进一步证实了PCOS女性可能存在昼夜节律紊乱101。一项针对青春期女孩的横断研究指出,基于褪黑激素分泌不规则的早晨昼夜节律失调与PCOS相关的代谢紊乱之间存在关系102。
一项随机、双盲、安慰剂对照试验对84名PCOS女性进行了研究,发现每天服用6mg褪黑激素和250mg氧化镁,持续8周,与基线相比,减少了不必要的毛发生长、血清胰岛素、总睾酮、总胆固醇和LDL胆固醇,提高了HDL胆固醇和总抗氧化能力103,104。一项针对40名PCOS女性的前瞻性队列研究发现,补充褪黑激素可降低男性激素水平,使其他生殖激素正常化,并改善月经规律105。在一项随机对照试验中,526名患有PCOS相关不孕症的妇女,在肌醇治疗的基础上每天添加3mg褪黑素可改善体外授精(IVF)前后的卵子质量106。
15.亚麻籽和亚麻籽油:
亚麻籽是木脂素(调节雌激素活性的植物化合物)和α-亚麻酸(ω-3脂肪酸)的来源。在动物模型中,亚麻籽油被发现可以调节激素信号传导,改善脂质代谢,并部分通过改变肠道微生物组组成来减少与PCOS相关的炎症107-109。亚麻籽粉也是膳食纤维的来源,这也可能对PCOS有益。
在一项由41名PCOS患者完成的随机、开放标签对照试验中,那些改变生活方式并在12周内每天服用30g亚麻籽粉(约2汤匙)的患者与单独改变生活方式相比,表现出了一些改善。这些变化包括体重、胰岛素抵抗、甘油三酯、hs-CRP、瘦素(一种食欲调节激素,其高水平通常与肥胖有关)、HDL胆固醇和脂联素的改善110。在一份病例报告中,在一名31岁的PCOS患者中,连续四个月每天30g亚麻籽粉与雄激素水平降低和不必要的毛发生长有关109。
更多内容可点击其个性化综合干预方案如下:
注意:需要了解多囊卵巢综合征与生育关系,可点击本网专文:
参阅本网如下专文了解更多相关内容:
医疗干预
治疗需要根据患者是否想要怀孕而不同。治疗的目标,首先是针对伴有PCOS的潜在胰岛素抵抗。
其他治疗措施可包括如下:
参考文献:
1. Sortino MA et al. Polycystic Ovary Syndrome: Insights into the Therapeutic Approach with Inositols. Front Pharmacol. 2017;8:341.
2. Kamenov Z et al. Inositols in PCOS. Molecules. Nov 27 2020;25(23)
3. Monastra G et al. PCOS and Inositols: Controversial Results and Necessary Clarifications. Basic Differences Between D-Chiro and Myo-Inositol. Front Endocrinol (Lausanne). 2021;12:660381.
4. Caputo M et al. Inositols and metabolic disorders: From farm to bedside. Journal of traditional and complementary medicine. May 2020;10(3):252-259.
5. Watkins OC et al. A review of the role of inositols in conditions of insulin dysregulation and in uncomplicated and pathological pregnancy. Crit Rev Food Sci Nutr. Dec 7 2020:1-49.
6. Unfer V et al. Myo-inositol effects in women with PCOS: a meta-analysis of randomized controlled trials. Endocr Connect. Nov 2017;6(8):647-658.
7. Regidor PA et al. Management of women with PCOS using myo-inositol and folic acid. New clinical data and review of the literature. Hormone molecular biology and clinical investigation. Mar 2 2018;34(2)
8. Facchinetti F et al. Short-term effects of metformin and myo-inositol in women with polycystic ovarian syndrome (PCOS): a meta-analysis of randomized clinical trials. Gynecological endocrinology. Mar 2019;35(3):198-206.
9. Agrawal A et al. Comparison of metformin plus myoinositol vs metformin alone in PCOS women undergoing ovulation induction cycles: randomized controlled trial. Gynecological endocrinology. Jun 2019;35(6):511-514.
10. Prabhakar P et al. Impact of myoinositol with metformin and myoinositol alone in infertile PCOS women undergoing ovulation induction cycles - randomized controlled trial. Gynecological endocrinology. Apr 2021;37(4):332-336.
11. Lagana AS et al. Myo-inositol supplementation reduces the amount of gonadotropins and length of ovarian stimulation in women undergoing IVF: a systematic review and meta-analysis of randomized controlled trials. Archives of gynecology and obstetrics. Oct 2018;298(4):675-684.
12. Davinelli S et al. Targeting Metabolic Consequences of Insulin Resistance in Polycystic Ovary Syndrome by D-chiro-inositol and Emerging Nutraceuticals: A Focused Review. J Clin Med. Apr 2 2020;9(4)
13. Gambioli R et al. The use of D-chiro-Inositol in clinical practice. Eur Rev Med Pharmacol Sci. Jan 2021;25(1):438-446.
14. Nordio M et al. The 40:1 myo-inositol/D-chiro-inositol plasma ratio is able to restore ovulation in PCOS patients: comparison with other ratios. Eur Rev Med Pharmacol Sci. Jun 2019;23(12):5512-5521.
15. Benelli E et al. A Combined Therapy with Myo-Inositol and D-Chiro-Inositol Improves Endocrine Parameters and Insulin Resistance in PCOS Young Overweight Women. International journal of endocrinology. 2016;2016:3204083.
16. Le Donne M et al. Effects of three treatment modalities (diet, myoinositol or myoinositol associated with D-chiro-inositol) on clinical and body composition outcomes in women with polycystic ovary syndrome. Eur Rev Med Pharmacol Sci. Mar 2019;23(5):2293-2301.
17. Mendoza N et al. High dose of d-chiro-inositol improves oocyte quality in women with polycystic ovary syndrome undergoing ICSI: a randomized controlled trial. Gynecological endocrinology. May 2020;36(5):398-401.
18. Chandil N et al. Comparison of Metformin and N Acetylcysteine on Clinical, Metabolic Parameter and Hormonal Profile in Women with Polycystic Ovarian Syndrome. J Obstet Gynaecol India. Feb 2019;69(1):77-81.
19. El Sharkwy IA et al. Randomized controlled trial of N-acetylcysteine versus l-carnitine among women with clomiphene-citrate-resistant polycystic ovary syndrome. International journal of gynaecology and obstetrics. Oct 2019;147(1):59-64.
20. Nemati M et al. Comparison of metformin and N-acetyl cysteine, as an adjuvant to clomiphene citrate, in clomiphene-resistant women with polycystic ovary syndrome. J Gynecol Obstet Hum Reprod. Sep 2017;46(7):579-585.
21. Mostajeran F et al. N-Acetylcysteine as an Adjuvant to Letrozole for Induction of Ovulation in Infertile Patients with Polycystic Ovary Syndrome. Advanced biomedical research. 2018;7:100.
22. Behrouzi Lak T et al. N-acetyl cysteine in ovulation induction of PCOS women underwent intrauterine insemination: An RCT. Int J Reprod Biomed. Apr 2017;15(4):203-208.
23. Cheraghi E et al. N-Acetylcysteine Compared to Metformin, Improves The Expression Profile of Growth Differentiation Factor-9 and Receptor Tyrosine Kinase c-Kit in The Oocytes of Patients with Polycystic Ovarian Syndrome. Int J Fertil Steril. Jan 2018;11(4):270-278.
24. Muscogiuri G et al. Shedding new light on female fertility: The role of vitamin D. Rev Endocr Metab Disord. Sep 2017;18(3):273-283.
25. Mu Y. Vitamin D and Polycystic Ovary Syndrome: a Narrative Review. Reprod Sci. Aug 2021;28(8):2110-2117.
26. Kalyanaraman R et al. A Narrative Review of Current Understanding of the Pathophysiology of Polycystic Ovary Syndrome: Focus on Plausible Relevance of Vitamin D. Int J Mol Sci. May 5 2021;22(9)
27. Davis EM et al. Associations between vitamin D levels and polycystic ovary syndrome phenotypes. Minerva endocrinologica. Jun 2019;44(2):176-184.
28. Kumar A et al. Correlation of Vitamin D with metabolic parameters in polycystic ovarian syndrome. J Family Med Prim Care. Jan-Mar 2017;6(1):115-119.
29. Miao CY et al. Effect of vitamin D supplementation on polycystic ovary syndrome: A meta-analysis. Exp Ther Med. Apr 2020;19(4):2641-2649.
30. Jin B et al. Influence of vitamin D supplementation on lipid levels in polycystic ovary syndrome patients: a meta-analysis of randomized controlled trials. J Int Med Res. Aug 2020;48(8):300060520935313.
31. Guo S et al. Vitamin D Supplementation Ameliorates Metabolic Dysfunction in Patients with PCOS: A SystematicReview of RCTs and Insight into the Underlying Mechanism. International journal of endocrinology. 2020;2020:7850816.
32. Al-Bayyari N et al. Androgens and hirsutism score of overweight women with polycystic ovary syndrome improved after vitamin D treatment: A randomized placebo controlled clinical trial. Clin Nutr. Mar 2021;40(3):870-878.
33. Salek M et al. N-3 fatty acids as preventive and therapeutic agents in attenuating PCOS complications. Excli j. 2019;18:558-575.
34. Lu L et al. Dietary and serum omega-3 polyunsaturated fatty acids and PCOS: A matched case-control study. Br J Nutr. 2022 Jul 14;128(1):114-123.
35. Yang K et al. Effectiveness of Omega-3 fatty acid for polycystic ovary syndrome: a systematic review and meta-analysis. Reproductive biology and endocrinology. Mar 27 2018;16(1):27.
36. ScienceDirect. Adiponectin. 12/3/2021. https://www.sciencedirect.com/topics/medicine-and-dentistry/adiponectin
37. Tosatti JAG et al. Influence of n-3 fatty acid supplementation on inflammatory and oxidative stress markers in patients with polycystic ovary syndrome: a systematic review and meta-analysis. Br J Nutr. Mar 28 2021;125(6):657-668.
38. Khani B et al. Omega-3 supplementation effects on polycystic ovary syndrome symptoms and metabolic syndrome. Journal of research in medical sciences. 2017;22:64.
39. Kostov K. Effects of Magnesium Deficiency on Mechanisms of Insulin Resistance in Type 2 Diabetes: Focusing on the Processes of Insulin Secretion and Signaling. Int J Mol Sci. Mar 18 2019;20(6)
40. Babapour M et al. Associations Between Serum Magnesium Concentrations and Polycystic Ovary Syndrome Status: a Systematic Review and Meta-analysis. Biol Trace Elem Res. Apr 2021;199(4):1297-1305.
41. Luo X et al. Associations of Serum Magnesium With Insulin Resistance and Testosterone in Women With Polycystic Ovary Syndrome. Front Endocrinol (Lausanne). 2021;12:683040.
42. Farsinejad-Marj M et al. Clinical and Metabolic Responses to Magnesium Supplementation in Women with Polycystic Ovary Syndrome. Biol Trace Elem Res. Aug 2020;196(2):349-358.
43. Higdon J. Lipoic Acid. Linus Pauling Institute. Updated 1/2019, https://lpi.oregonstate.edu/mic/dietary-factors/lipoic-acid#summary
44. Mahmoudi-Nezhad M et al. An updated systematic review and dose-response meta-analysis of the effects of α-lipoic acid supplementation on glycemic markers in adults. Nutrition. Feb 2021;82:111041.
45. Genazzani AD et al. Modulatory effects of alpha-lipoic acid (ALA) administration on insulin sensitivity in obese PCOS patients. J Endocrinol Invest. May 2018;41(5):583-590.
46. Masharani U et al. Effects of controlled-release alpha lipoic acid in lean, nondiabetic patients with polycystic ovary syndrome. J Diabetes Sci Technol. Mar 1 2010;4(2):359-64.
47. Cirillo F et al. HMGB1 is increased in adolescents with polycystic ovary syndrome (PCOS) and decreases after treatment with myo-inositol (MYO) in combination with alpha-lipoic acid (ALA). Gynecological endocrinology. Jul 2020;36(7):588-593.
48. De Cicco S et al. Myoinositol combined with alpha-lipoic acid may improve the clinical and endocrine features of polycystic ovary syndrome through an insulin-independent action. Gynecological endocrinology. Sep 2017;33(9):698-701.
49. Fruzzetti F et al. Long-term treatment with alpha-lipoic acid and myo-inositol positively affects clinical and metabolic features of polycystic ovary syndrome. Gynecological endocrinology. Feb 2020;36(2):152-155.
50. Fruzzetti F et al. Clinical and Metabolic Effects of Alpha-Lipoic Acid Associated with Two Different Doses of Myo-Inositol in Women with Polycystic Ovary Syndrome. International journal of endocrinology. 2020;2020:2901393.
51. Piotrowska A et al. The Possibilities of Using Chromium Salts as an Agent Supporting Treatment of Polycystic Ovary Syndrome. Biol Trace Elem Res. Dec 2019;192(2):91-97.
52. Zaeemzadeh N et al. Comparison of dietary micronutrient intake in PCOS patients with and without metabolic syndrome. Journal of ovarian research. Jan 9 2021;14(1):10.
53. Ashoush S et al. Chromium picolinate reduces insulin resistance in polycystic ovary syndrome: Randomized controlled trial. J Obstet Gynaecol Res. Mar 2016;42(3):279-85.
54. Lucidi RS et al. Effect of chromium supplementation on insulin resistance and ovarian and menstrual cyclicity in women with polycystic ovary syndrome. Fertility and sterility. Dec 2005;84(6):1755-7.
55. Lydic ML et al. Chromium picolinate improves insulin sensitivity in obese subjects with polycystic ovary syndrome. Fertility and sterility. Jul 2006;86(1):243-6.
56. Fazelian S et al. Chromium supplementation and polycystic ovary syndrome: A systematic review and meta-analysis. Journal of trace elements in medicine and biology : organ of the Society for Minerals and Trace Elements (GMS). Jul 2017;42:92-96.
57. Tang XL et al. Chromium supplementation in women with polycystic ovary syndrome: Systematic review and meta-analysis. J Obstet Gynaecol Res. Jan 2018;44(1):134-143.
58. Bene J et al. Role of carnitine and its derivatives in the development and management of type 2 diabetes. Nutr Diabetes. Mar 7 2018;8(1):8. doi:10.1038/s41387-018-0017-1
59. Savic D et al. The Importance of the Fatty Acid Transporter L-Carnitine in Non-Alcoholic Fatty Liver Disease (NAFLD). Nutrients. Jul 22 2020;12(8)
60. Celik F et al. Plasma L-carnitine levels of obese and non-obese polycystic ovary syndrome patients. J Obstet Gynaecol. May 2017;37(4):476-479.
61. Salehpour S et al. Effects of L-carnitine on Polycystic Ovary Syndrome. JBRA Assist Reprod. Oct 14 2019;23(4):392-395.
62. Ismail AM et al. Adding L-carnitine to clomiphene resistant PCOS women improves the quality of ovulation and the pregnancy rate. A randomized clinical trial. European journal of obstetrics, gynecology, and reproductive biology. Sep 2014;180:148-52.
63. Tauqir S et al. Acetyl-L-Carnitine Ameliorates Metabolic and Endocrine Alterations in Women with PCOS: A Double-Blind Randomized Clinical Trial. Adv Ther. Jul 2021;38(7):3842-3856.
64. He FF et al. Role of gut microbiota in the development of insulin resistance and the mechanism underlying polycystic ovary syndrome: a review. Journal of ovarian research. Jun 17 2020;13(1):73.
65. Li Y et al. Effects of probiotics, prebiotics, and synbiotics on polycystic ovary syndrome: a systematic review and meta-analysis. Crit Rev Food Sci Nutr. Jul 21 2021:1-17.
66. Cozzolino M et al. Therapy with probiotics and synbiotics for polycystic ovarian syndrome: a systematic review and meta-analysis. Eur J Nutr. Oct 2020;59(7):2841-2856.
67. Karimi E et al. The effect of synbiotics supplementation on anthropometric indicators and lipid profiles in women with polycystic ovary syndrome: a randomized controlled trial. Lipids in health and disease. Apr 6 2020;19(1):60.
68. Tillhon M et al. Berberine: new perspectives for old remedies. Biochem Pharmacol. Nov 15 2012;84(10):1260-7.
69. Rondanelli M et al. Berberine Phospholipid Is an Effective Insulin Sensitizer and Improves Metabolic and Hormonal Disorders in Women with Polycystic Ovary Syndrome: A One-Group Pretest-Post-Test Explanatory Study. Nutrients. 2021;13(10):3665.
70. Li MF et al. The Effect of Berberine on Polycystic Ovary Syndrome Patients with Insulin Resistance (PCOS-IR): A Meta-Analysis and Systematic Review. Evid Based Complement Alternat Med. 2018;2018:2532935.
71. Wang Z et al. Berberine improves ovulation and endometrial receptivity in polycystic ovary syndrome. Phytomedicine. Oct 2021;91:153654.
72. Zhang SW et al. Effect and mechanism of berberine against polycystic ovary syndrome. Biomed Pharmacother. Jun 2021;138:111468.
73. Wei W et al. A clinical study on the short-term effect of berberine in comparison to metformin on the metabolic characteristics of women with polycystic ovary syndrome. Eur J Endocrinol. Jan 2012;166(1):99-105.
74. An Y et al. The use of berberine for women with polycystic ovary syndrome undergoing IVF treatment. Clin Endocrinol (Oxf). Mar 2014;80(3):425-31.
75. Yu J et al. Protective effects of berberine in a rat model of polycystic ovary syndrome mediated via the PI3K/AKT pathway. J Obstet Gynaecol Res. May 2021;47(5):1789-1803.
76. Shen HR et al. Berberine exerts a protective effect on rats with polycystic ovary syndrome by inhibiting the inflammatory response and cell apoptosis. Reproductive biology and endocrinology : RB&E. Jan 7 2021;19(1):3.
77. Kysenius K et al. Mitochondria and NMDA receptor-dependent toxicity of berberine sensitizes neurons to glutamate and rotenone injury. PLoS One. 2014;9(9):e107129. doi:10.1371/journal.pone.0107129
78. Mikes V, Dadák V. Berberine derivatives as cationic fluorescent probes for the investigation of the energized state of mitochondria. Biochim Biophys Acta. May 27 1983;723(2):231-9.
79. Mikes V et al. Interaction of fluorescent berberine alkyl derivatives with respiratory chain of rat liver mitochondria. J Bioenerg Biomembr. Feb 1985;17(1):23-32.
80. Santos HO et al. To what extent does cinnamon administration improve the glycemic and lipid profiles? Clin Nutr ESPEN. Oct 2018;27:1-9.
81. Mollazadeh H et al. Cinnamon effects on metabolic syndrome: a review based on its mechanisms. Iranian journal of basic medical sciences. Dec 2016;19(12):1258-1270.
82. Shirzad F et al. Cinnamon effects on blood pressure and metabolic profile: A double-blind, randomized, placebo-controlled trial in patients with stage 1 hypertension. Avicenna journal of phytomedicine. Jan-Feb 2021;11(1):91-100.
83. Heshmati J et al. The effect of cinnamon supplementation on glycemic control in women with polycystic ovary syndrome: A systematic review and meta-analysis. J Food Biochem. Jan 2021;45(1):e13543.
84. Hajimonfarednejad M et al. Insulin resistance improvement by cinnamon powder in polycystic ovary syndrome: A randomized double-blind placebo controlled clinical trial. Phytother Res. Feb 2018;32(2):276-283.
85. Borzoei A et al. Effects of cinnamon supplementation on antioxidant status and serum lipids in women with polycystic ovary syndrome. Journal of traditional and complementary medicine. Jan 2018;8(1):128-133.
86. Dou L et al. The effect of cinnamon on polycystic ovary syndrome in a mouse model. Reproductive biology and endocrinology. Oct 19 2018;16(1):99.
87. Den Hartogh DJ et al. Antidiabetic Properties of Curcumin II: Evidence from In Vivo Studies. Nutrients. Dec 25 2019;12(1)
88. Chien YJ et al. Effects of Curcumin on Glycemic Control and Lipid Profile in Polycystic Ovary Syndrome: Systematic Review with Meta-Analysis and Trial Sequential Analysis. Nutrients. Feb 21 2021;13(2)
89. Sohaei S et al. The effects of curcumin supplementation on glycemic status, lipid profile and hs-CRP levels in overweight/obese women with polycystic ovary syndrome: A randomized, double-blind, placebo-controlled clinical trial. Complement Ther Med. Dec 2019;47:102201.
90. Heshmati J et al. Effects of curcumin supplementation on blood glucose, insulin resistance and androgens in patients with polycystic ovary syndrome: A randomized double-blind placebo-controlled clinical trial. Phytomedicine. Jan 2021;80:153395.
91. Heshmati J et al. The effects of curcumin supplementation on oxidative stress, Sirtuin-1 and peroxisome proliferator activated receptor gamma coactivator 1alpha gene expression in polycystic ovarian syndrome (PCOS) patients: A randomized placebo-controlled clinical trial. Diabetes Metab Syndr. Mar - Apr 2020;14(2):77-82.
92. Cai X et al. Phytoestrogens for the Management of Endometriosis: Findings and Issues. Pharmaceuticals (Basel). Jun 14 2021;14(6)
93. Pasquariello R et al. The Role of Resveratrol in Mammalian Reproduction. Molecules. Oct 5 2020;25(19)
94. Shojaei-Zarghani S et al. Resveratrol and Markers of Polycystic Ovary Syndrome: a Systematic Review of Animal and Clinical Studies. Reprod Sci. 2022 Sep;29(9):2477-2487.
95. Mansour A et al. Effect of resveratrol on menstrual cyclicity, hyperandrogenism and metabolic profile in women with PCOS. Clin Nutr. Jun 2021;40(6):4106-4112.
96. Banaszewska B et al. Effects of Resveratrol on Polycystic Ovary Syndrome: A Double-blind, Randomized, Placebo-controlled Trial. J Clin Endocrinol Metab. Nov 2016;101(11):4322-4328.
97. Bahramrezaie M et al. Effects of resveratrol on VEGF & HIF1 genes expression in granulosa cells in the angiogenesis pathway and laboratory parameters of polycystic ovary syndrome: a triple-blind randomized clinical trial. J Assist Reprod Genet. Aug 2019;36(8):1701-1712.
98. Brenjian S et al. Resveratrol treatment in patients with polycystic ovary syndrome decreased pro-inflammatory and endoplasmic reticulum stress markers. Am J Reprod Immunol. Jan 2020;83(1):e13186.
99. Kunitomi C, Harada M, Kusamoto A, et al. Induction of aryl hydrocarbon receptor in granulosa cells by endoplasmic reticulum stress contributes to pathology of polycystic ovary syndrome. Mol Hum Reprod. Feb 27 2021;27(3)
100. Spinedi E et al. The Polycystic Ovary Syndrome and the Metabolic Syndrome: A Possible Chronobiotic-Cytoprotective Adjuvant Therapy. International journal of endocrinology. 2018;2018:1349868.
101. Lim AJR et al. Phenotypic spectrum of polycystic ovary syndrome and their relationship to the circadian biomarkers, melatonin and cortisol. Endocrinol Diabetes Metab. Jul 2019;2(3):e00047.
102. Simon SL et al. Morning Circadian Misalignment Is Associated With Insulin Resistance in Girls With Obesity and Polycystic Ovarian Syndrome. J Clin Endocrinol Metab. Aug 1 2019;104(8):3525-3534.
103. Alizadeh M et al. Metabolic and hormonal effects of melatonin and/or magnesium supplementation in women with polycystic ovary syndrome: a randomized, double-blind, placebo-controlled trial. Nutr Metab (Lond). Jun 6 2021;18(1):57.
104. Mousavi R et al. Effects of Melatonin and/or Magnesium Supplementation on Biomarkers of Inflammation and Oxidative Stress in Women with Polycystic Ovary Syndrome: a Randomized, Double-Blind, Placebo-Controlled Trial. Biol Trace Elem Res. 2022 Mar;200(3):1010-1019.
105. Tagliaferri V et al. Melatonin Treatment May Be Able to Restore Menstrual Cyclicity in Women With PCOS: A Pilot Study. Reprod Sci. Feb 2018;25(2):269-275.
106. Pacchiarotti A et al. Effect of myo-inositol and melatonin versus myo-inositol, in a randomized controlled trial, for improving in vitro fertilization of patients with polycystic ovarian syndrome. Gynecological endocrinology. 2016;32(1):69-73.
107. Wang T et al. Dietary α-Linolenic Acid-Rich Flaxseed Oil Exerts Beneficial Effects on Polycystic Ovary Syndrome Through Sex Steroid Hormones-Microbiota-Inflammation Axis in Rats. Front Endocrinol (Lausanne). 2020;11:284.
108. Komal F et al. Impact of different omega-3 fatty acid sources on lipid, hormonal, blood glucose, weight gain and histopathological damages profile in PCOS rat model. J Transl Med. Sep 14 2020;18(1):349.
109. Nowak DA et al. The Effect of Flaxseed Supplementation on Hormonal Levels Associated with Polycystic Ovarian Syndrome: A Case Study. Curr Top Nutraceutical Res. 2007;5(4):177-181.
110. Haidari F et al. The effects of flaxseed supplementation on metabolic status in women with polycystic ovary syndrome: a randomized open-labeled controlled clinical trial. Nutr J. Jan 24 2020;19(1):8.
美国梅奥诊所
www.mayoclinic.org
美国国立卫生研究院大众健康网
www.medlineplus.gov
美国多囊卵巢综合征协会
http://www.pcosupport.org
美国妇产科医师大会
http://www.acog.org
加拿大女性健康网
http://www.womenshealthmatters.ca
其他参考文献:详见具体的综合干预方案
免责声明和安全信息
英文名称:Polycystic Ovary Syndrome, PCOS;Polyfollicular Ovarian Appearance
定义
多囊卵巢综合征(PCOS)是一种常见的、最复杂的慢性内分泌疾病。卵巢生成卵泡,但卵泡不成熟、无法每月正常释放一个成熟的卵子。不成熟的卵泡可以变成充满液体的小囊,称为囊肿,这是PCOS由来。育龄妇女约有5-10%存在PCOS,并且影响到生殖功能或不孕。病因及可能机制
虽然PCOS的根本原因尚不清楚,但异常的胰岛素和激素分泌及信号传导似乎是关键因素。遗传、表观遗传和环境因素也可能起作用。- 促性腺激素和雄激素分泌及信号传导异常
促黄体生成素(LH)是刺激卵泡成熟的垂体激素之一,其分泌过多似乎在多囊卵巢综合征中发挥作用。LH、促卵泡激素(FSH)和促性腺激素释放激素(GnRH)的复杂相互作用似乎会导致雄激素分泌增加,并破坏卵泡的正常发育。与此同时,雄性激素水平过高会导致LH分泌过多。更为复杂的是,胰岛素水平过高—多囊卵巢综合征高发病率的另一个突出特征,也会导致高雄激素血症。
- 胰岛素分泌和信号异常
患有PCOS的女性容易出现胰岛素信号缺陷,这会导致体重增加和肥胖的风险,加剧卵巢和肾上腺中雄激素的过量产生。同时,过量的雄激素会引起胰岛素抵抗,导致脂肪组织信号功能失调,并进一步升高胰岛素水平,从而刺激体重增加和雄激素合成。其结果是激素和代谢症状恶化以及综合征进展的恶性循环。
- 性早熟(肾上腺初潮)
出现早熟迹象的女孩(8岁之前)通常有类似多囊卵巢综合征的体征和症状。事实上,已经发现青春期过早的迹象与雄激素分泌高和月经不规律有关,这表明青春期过早可能是多囊卵巢综合征的早期表现。
- 慢性炎症
慢性全身性炎症也被认为在PCOS中起作用。研究发现,患有PCOS的女性具有更高水平的炎症标志物,与她们的体重状况无关。脂肪组织的炎症信号失调以及卵巢、肝脏和其他组织的细胞因子和自由基会导致炎症状态,并进一步促进代谢失衡和胰岛素抵抗。炎症和氧化应激也会损害卵巢功能和卵泡成熟。
- 发育和早期生活暴露
一些证据表明,某些暴露会影响胎儿和未成熟卵巢的发育。其中包括子宫内暴露于高水平的雄激素,以及胎儿或儿童暴露于干扰激素的化学物质或药物。这甚至可能延伸到某些食物。其他母体因素,如妊娠期高血压、妊娠期糖尿病或吸烟,被认为是导致多囊卵巢综合征风险的因素,而儿童时期的环境因素,如不良饮食和缺乏运动,可能会加剧这种风险。
风险因素
可能增加多囊卵巢综合征发生的因素,包括如下:- 家庭成员患有PCOS
- 月经周期不规则
- 肥胖
- 发育期过早
- 久坐不动的生活方式
症状
有些妇女可能没有症状,而有些在15-30岁之间,可能出现症状。在有症状的女性中,PCOS可能引起如下:
- 月经失调或无月经、闭经
- 多毛症,雄激素过高导致脸部、身体毛发多
- 痤疮
- 不孕症
- 肥胖,尤其在腹部
- 发黑、增厚的皮肤斑块,在颈部、腹股沟和腋窝区
- 脱发、男性型秃头,头顶头发变稀
并发症
患有PCOS的妇女有增加下列并发症的风险:- 生殖问题如:
- 女性不孕症
- 妊娠期糖尿病、妊娠高血压
- 流产或早产
- 其他健康问题如下:
疗法
综合治疗包括如下:调整饮食与生活方式
- 健康均衡饮食,富含纤维如丰富蔬菜、水果和全谷类食物等
- 减少糖、淀粉等摄入
- 经常运动、锻炼,改善胰岛素抵抗
- 减肥,如果超重的话
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控多囊卵巢综合征的营养和草本补充剂,主要包括如下:
1.肌醇:
肌醇(Inositol)是一种存在于植物中的糖醇(纤维糖),并可在人体内产生,具有多种结构形式或异构体。其中,和肌醇(Myo-inositol)是自然界中分布最广泛的异构体,在卵巢中含量丰富。D-手性肌醇(DCI)异构体在体内的含量较少,有些和肌醇在体内转化为DCI1,2。
肌醇异构体以游离形式存在于细胞中,并作为膜磷脂的成分,在细胞间信号传导中具有活性1。此外,肌醇磷酸盐充当多种激素的第二信使,包括胰岛素和FSH,通过将外部信号传输到细胞的工作内部2-4。肌醇磷酸系统的失调与胰岛素抵抗和相关疾病有关,包括多囊卵巢综合征(PCOS)4,5。在临床试验中,和肌醇及DCI都对葡萄糖调节有积极作用;然而,和肌醇和DCI似乎对卵巢和垂体激素的产生有不同的影响,和肌醇与DCI治疗PCOS的最佳比例仍未确定3。
1.1.和肌醇(Myo-inositol,通称肌醇):
许多临床试验已经证明,和肌醇可以改善胰岛素敏感性和代谢标志物,也会影响PCOS女性的卵巢功能2,6,7。一项对6项随机对照试验(含355名参与者)的荟萃分析发现,与二甲双胍相比,和肌醇在对空腹胰岛素和胰岛素敏感性、睾酮、PCOS患者的性激素结合球蛋白(SHBG)和体重指数(BMI)的作用相当,而二甲双胍治疗的不良反应风险更高8。
补充和肌醇也被证明可以提高生育能力。一项随机对照试验对120名接受促排卵的PCOS相关的不孕妇女进行了为期三个月的每日二甲双胍加1800mg肌醇与单独二甲双胍的比较。与单独使用二甲双胍治疗的妇女相比,接受二甲双胍和肌醇治疗的妇女的成功分娩率增加了一倍多(分别为55%和27%)9。另一项针对116名PCOS相关不孕症妇女的随机对照试验发现,与同时接受肌醇和二甲双胍治疗的妇女相比,每天接受4g肌醇治疗6个月的女性在代谢标志物和激素水平方面有相当的改善。与单独使用肌醇相比,添加二甲双胍对受孕没有显著优势。二甲双胍组的副作用更多,主要是胃肠道副作用10。其他研究表明,在多囊卵巢综合征患者不孕治疗期间,补充肌醇可降低卵巢过度刺激综合征的风险7,11。
1.2. D-手性肌醇(DCI):
D-手性肌醇对介导胰岛素反应很重要,已被证明可以改善PCOS患者的胰岛素敏感性和改善与胰岛素抵抗相关的代谢状况12。通过恢复胰岛素活性,DCI补充剂可能有助于改善卵巢功能。然而,DCI也被发现可以抑制芳香化酶(一种促进卵巢中雄激素转化为雌激素的酶),并且发现更高剂量的DCI可以增加PCOS女性的循环睾酮水平3,13。此外,高剂量DCI可能会干扰肌醇的吸收,从而降低治疗效果的可能性,尽管目前还没有关于这种关系的结论性数据3。
1.3.和肌醇加D-手性肌醇:
由于二者的作用不同,和肌醇和DCI可能具有互补作用。建议将肌醇与DCI的比例定为40:1,因为这被认为反映了血浆中这些化合物的生理平衡3,14。一项针对56名PCOS患者的随机对照试验将使用七种不同配方的每天4g肌醇与单独DCI或肌醇与DCI的效果进行了比较,其比例如下:1:3.5、2.5:1、5:1、20:1、40:1,或80:1。和肌醇与DCI的比例为40:1,对恢复排卵和一系列生殖激素的正常水平最为有效,而所有配方都能改善代谢标志物14。
一项针对46名PCOS和肥胖参与者的随机对照试验,比较了六个月的和肌醇加DCI联合每日治疗的效果,其比例为40:1(含1100mg肌醇)加400mcg叶酸与每天400mcg单独叶酸。接受肌醇加DCI治疗的患者LH、游离睾酮和空腹胰岛素水平降低幅度更大,雌激素水平升高,胰岛素敏感性改善15。在另一项对44名超重或肥胖PCOS患者的对照试验中,10名患者接受饮食、4g肌醇和400mcg叶酸的治疗;13名以40:1的比例加入肌醇和DCI(含1,100mg肌醇);单独饮食组21名。在所有组中体重、BMI、臀围和腰围都显著下降,而只有比例为40:1的组月经规律得到了显著恢复16。
在一项对照试验中,对11名患有PCOS相关不孕并接受体外受精(IVF)的女性在接受550mg肌醇加每天300mg或27.6mg DCI治疗12周后获得的卵母细胞质量进行了评估。研究发现,更高剂量的DCI对卵母细胞质量有更大的积极影响17。
2. N-乙酰半胱氨酸(NAC):
已知NAC是含硫氨基酸半胱氨酸的一种形式,也是谷胱甘肽的前体,谷胱甘肽是人体内最重要的抗氧化剂和解毒剂之一。
一项针对100名PCOS受试者的随机对照试验将NAC(1800mg/天)和二甲双胍(1500mg/天)治疗24周进行了比较。NAC治疗显著改善了BMI、腰围和腰臀比,而二甲双胍则没有。此外,NAC显著改善了胰岛素敏感性标志物,如空腹胰岛素、空腹血糖和空腹血糖/胰岛素比值,但二甲双胍没有改善。NAC治疗的参与者的总睾酮水平下降幅度更大,副作用更少18。
多项对照试验表明,NAC可以提高促排卵药物对多囊卵巢综合征不孕妇女的疗效。在一项随机对照试验中,162名接受生育药物柠檬酸克罗米芬(Clomid)治疗失败的PCOS相关不孕症妇女比较了在治疗中添加NAC或L肉碱三个月的效果。NAC组在游离睾酮水平和胰岛素抵抗标志物方面有更大的改善,而两组在月经规律、LH和FSH水平方面都有类似的改善;然而,只有L-肉碱组的血脂水平有所改善19。在另一项对照试验中,将每天1800mg NAC与1500mg二甲双胍作为克罗米芬柠檬酸盐治疗的补充,对108名克罗米芬耐药PCOS相关不孕妇女进行了比较。NAC导致不想要的头发生长和空腹血糖水平的大幅下降;二甲双胍使BMI和胰岛素水平显著降低。此外,NAC和二甲双胍对12周后的排卵率和生育率也有类似的积极作用20。
NAC也可能有助于接受来曲唑(Femara)不孕治疗的妇女。一项针对130名PCOS患者的双盲、随机、安慰剂对照试验显示,与单独使用来曲唑或安慰剂相比,来曲唑联合每天1200mg NAC可在5天后产生更多直径大于18mm(与排卵可能性较大相关)的卵泡。此外,接受NAC作为来曲唑辅助治疗的患者排卵率和妊娠率较高21。然而,另一项包括97名PCOS患者的随机对照试验发现,每天1200mg NAC并不能改善克罗米芬和来曲唑联合治疗的促排卵效果22。
NAC作为试管婴儿之前的支持性治疗也可能有价值。在一项对80名准备试管婴儿的PCOS妇女进行的安慰剂对照试验中,每天1800mg NAC持续六周似乎可以改善卵细胞的质量23。
3. 维生素D:
维生素D在生殖和代谢健康中的重要作用越来越受到人们的认可,维生素D缺乏可能会导致PCOS女性的激素、代谢和心理健康障碍24-26。一项观察性研究发现,维生素D不足与PCOS女性较高的雄性激素水平和BMI有关,另一项研究发现,维生素D缺乏症在患有PCOS的女性中比没有PCOS的女性更常见27,28。
多项随机对照试验和荟萃分析表明,维生素D治疗对PCOS妇女的代谢和激素健康有有益影响。一项荟萃分析包括了11项随机对照试验的数据,这些试验共涉及483名PCOS女性。该荟萃分析发现,维生素D的剂量范围为每天4000–7143IUs(100–179mcg),可降低总睾酮、胰岛素抵抗、总胆固醇和LDL胆固醇29。对许多相同试验的其他荟萃分析也得出了类似的结论,发现维生素D对PCOS女性,特别是维生素D缺乏症女性的脂质代谢和葡萄糖代谢有广泛的积极影响。
在一项为期12周的随机安慰剂对照试验中,30名患有PCOS和维生素D缺乏症的超重女性(18-49岁)每周服用50,000IU(1250 mcg)维生素D,补充维生素D可减少多余的头发生长和雄性激素水平30,31。在另一项随机对照试验中包括180名患有PCOS的女性和150名未患有PCOS女性,所有患者的血清25-OH维生素D水平均低于30ng/mL,而那些每周接受20,000 IU(500mcg)维生素D的PCOS患者的LH:FSH比率与安慰剂相比有所改善32。
4. 欧米伽3脂肪酸:
ω-3脂肪酸的抗炎活性可以减少PCOS的心血管、代谢和激素并发症33。一项针对325名PCOS女性和325名健康对照的病例对照研究发现,PCOS女性血清磷脂中的ω-3脂肪含量较低。ω-3含量最高的三分之一的女性患多囊卵巢综合征的几率比含量最低的三分之一的女性低30-40%34。
一项包括9项随机对照试验的统计分析,共涉及591名PCOS女性,还报告发现补充ω-3脂肪酸可以改善胰岛素敏感性,降低总胆固醇和甘油三酯水平,以及脂联素(一种主要由脂肪组织产生的信号肽,可提高胰岛素敏感性并具有抗炎特性)水平35,36。另一项统计分析发现,补充Omega-3脂肪酸可降低PCOS女性的高敏C反应蛋白(hs-CRP)水平,增加脂联素水平37。
在一项针对88名PCOS女性的随机对照试验中,连续六个月每天补充2000mg鱼油中的ω-3脂肪酸(包括360mg EPA和240mg DHA),可降低腰围、甘油三酯和胆固醇水平38。
5. 镁:
镁在调节葡萄糖代谢和胰岛素敏感性方面起着重要作用,低镁状态可能是胰岛素抵抗发展为2型糖尿病和心脏病的一个促成因素39。对总共2000多名女性的8项研究进行的统计分析发现,患有PCOS的超重或肥胖女性的血清镁浓度低于患有PCOS的正常体重女性40。此外,一项对1000多名PCOS患者的镁状况进行调查的研究发现,镁水平越低,胰岛素抵抗越差,睾酮水平越高41。
另一项针对60名PCOS患者的安慰剂对照试验发现,连续8周每天250mg氧化镁可增加LH水平并降低BMI,但不会影响葡萄糖或脂质代谢标志物或多种激素状态指数42。
6. 硫辛酸:
硫辛酸(ALA)是一种重要的抗氧化营养素,已被证明可支持健康的葡萄糖代谢43。一项大型统计分析发现,ALA可降低血清胰岛素并提高胰岛素敏感性44。在一项针对32名PCOS和肥胖女性的非对照试验中,每天400mg ALA治疗12周可降低胰岛素和葡萄糖水平、BMI和胰岛素抵抗45。在另一项小型非对照试验中,6名患有PCOS的正常体重女性服用600mg控释硫辛酸,每天两次,持续16周。胰岛素抵抗、甘油三酯水平和低密度脂蛋白颗粒大小得到改善。此外,未服用口服避孕药的两名受试者的月经不规律也有所改善46。
几项临床试验已经注意到硫辛酸和肌醇的组合对PCOS的生物标志物和症状的积极影响。在一项针对23名PCOS青少年和21名健康对照的病例对照研究中,研究了肌醇加硫辛酸治疗6个月。治疗显著降低了胰岛素抵抗和血清胰岛素水平47。在一项针对40名PCOS女性的非对照试点研究中,肌醇和硫辛酸的组合降低了雄性激素水平,改善了月经规律,在不影响葡萄糖或胰岛素参数的情况下,减少了多余的头发生长和BMI48。在一项对44名月经不频繁的PCOS患者进行的非对照试验中,每天800mg硫辛酸和2000mg肌醇进行24个月的长期治疗,显著减少了月经不规律49。在一项针对71名PCOS女性的为期六个月的非对照试验中,每天800mg ALA加1000或2000mg肌醇改善了月经规律。然而,从中受益的1000mg的女性要少得多50。
7.铬:
矿物铬由于其支持葡萄糖调节和代谢健康的能力,可能对PCOS妇女有益51。一项针对42名PCOS妇女(14名患有代谢综合征,28名未患有)的病例对照研究发现,代谢综合征和PCOS的参与者铬和几种抗氧化微量营养素的摄入量较低52。
在一项双盲、随机、对照试验中,85名患有PCOS女性在六个月内每天接受1000mcg吡啶甲酸铬或安慰剂治疗,补充吡啶甲酸铬可显著改善BMI和空腹血清胰岛素水平。补充铬也使五个月后排卵和月经规律的机会增加了近两倍53。在一项小型试点试验中,该试验招募了10名PCOS女性,并将她们随机分组,每天接受200mcg吡啶甲酸铬或安慰剂治疗,为期四个月,补充铬改善了葡萄糖耐量,但没有改善排卵频率54。另一项小型研究也报道了患有PCOS的肥胖女性补充1000mcg吡啶甲酸铬后葡萄糖代谢的改善55。
对七项随机对照试验数据的统计分析发现,补充铬显著降低了BMI和游离睾酮水平56。然而,另一项荟萃分析包括6项随机对照试验,共有351名参与者,发现尽管补充铬降低了胰岛素抵抗,但也显著提高了总睾酮和游离睾酮水平57。基于这些关于游离睾酮水平的荟萃分析得出的不同结论,对于选择服用铬的PCOS女性来说,定期监测她们的游离睾酮水平是谨慎的。
8. L-肉碱:
L-肉碱是一种在脂质代谢中起关键作用的氨基酸。临床证据表明,它可能有助于治疗代谢紊乱,如2型糖尿病和非酒精性脂肪肝(NAFLD)58,59。一项观察性研究发现,患有PCOS的女性,尤其是肥胖女性,其L-肉碱水平低于无PCOS的女性60。
在一项针对74名PCOS妇女的非对照试验中,在三个月的时间里,每天服用3g L-肉碱可显著改善胰岛素敏感性、BMI、多余的头发生长、脂质水平和月经周期规律61。一项随机对照试验纳入了170名PCOS相关不孕妇女,她们已被证明对克罗米芬的作用具有耐药性。参与者被随机分配在月经周期的第3-7天接受150mg克罗米芬、安慰剂或3g L-肉碱的治疗。与安慰剂相比,L肉碱提高了排卵率(64.4%对17.4%)和妊娠率(51.5%对5.8%)62。
在一项针对147名PCOS女性的随机安慰剂对照试验中,发现乙酰L肉碱(ALC)形式的L肉碱,剂量为500mg,每日两次,可增加抗糖尿病药物二甲双胍和吡格列酮(Actos)的益处。一组只接受药物治疗,另一组接受药物加ALC治疗,第三组接受安慰剂治疗。两种积极治疗都导致血清胰岛素水平下降,尽管在接受ALC的组中效果更为明显。促黄体生成素(LH)降低,心理评分提高,也以类似的方式。两种治疗都能提高血清脂联素和胰岛素敏感性,并提高睾酮和FSH水平。只有接受ALC治疗的患者月经规律和腰围才有所改善63。
9.益生菌:
肠道微生物组在调节免疫功能和代谢方面发挥着关键作用,并可能在PCOS中不必要的毛发生长中发挥作用64。对17项随机对照试验的统计分析发现,摄入益生菌、益生元或合生元(益生菌加益生元)对PCOS的代谢方面有益。具体而言,空腹血糖和胰岛素水平、胰岛素敏感性、总胆固醇和LDL胆固醇以及甘油三酯水平均有改善65。另一项对共有587名参与者的9项随机对照试验结果的统计分析发现,使用益生菌或合生元治疗8周或更长时间,可以改善多余的头发生长、空腹血糖和胰岛素、胰岛素敏感性和BMI。此外,睾酮以及炎症和氧化应激指标也有所改善66。
然而,在一项针对99名PCOS患者的安慰剂对照试验中,提供益生元菊粉的合生元补充剂加上七种益生菌菌株的组合治疗12周,可以改善LDL和HDL胆固醇水平,但没有改变甘油三酯水平、体重或身体成分67。
10.黄连素:
黄连素(又称小檗碱)是一种生物活性生物碱,存在于包括伏牛、白毛茛等几种药用植物中68。这些植物已被广泛用于亚洲传统医学中治疗感染、代谢紊乱和其他适应症。黄连素在改善胰岛素敏感性、降低血清雄激素和调节慢性炎症方面的疗效使其成为多囊卵巢综合征研究的一个主题69-72。91-94
一项针对89名患有PCOS和胰岛素抵抗的女性的试验发现,与二甲双胍或安慰剂以及相同激素治疗的组合相比,黄连素与激素治疗相结合,可以改善脂质状况和SHBG水平,以及糖代谢和腰围73。在一项小型临床试验中,12名新诊断为PCOS妇女服用550mg黄连素磷脂复合物,每天两次,持续60天。治疗后,胰岛素敏感性、睾酮水平和炎症标志物显著改善69。黄连素也可能改善体外受精结果:150名接受体外受精治疗的PCOS妇女在卵巢刺激前随机接受二甲双胍、黄连素或安慰剂治疗三个月。与安慰剂组相比,服用二甲双胍或黄连素的女性睾酮和胰岛素抵抗降低,妊娠率增加。与二甲双胍相比,服用黄连素的妇女活产率也有所提高,不良反应更少74。
黄连素被认为通过抑制PI3K/AKT和MAPK途径、激活AMPK以及与多种其他靶点相互作用来影响激素水平和胰岛素代谢72,75。此外,黄连素可以通过降低几种促炎标志物的水平来改善PCOS病理的某些方面,如核因子κB(NF-κB)、肿瘤坏死因子α,以及白细胞介素1(IL-1)和6(IL-6)76。
尽管在人体临床试验中对黄连素进行了研究,并证明其具有多种代谢益处,但在某些临床前研究的基础上,人们对长期使用黄连素表示担忧77-79。一些证据表明,长期使用黄连素,尤其是高剂量的黄连素,可能会损害特定类型细胞中细胞代谢的某些方面。这项临床前研究的意义尚待长期人体临床试验确定。因此,目前建议短期使用黄连素为宜。
11.肉桂:
对多项临床试验的一项综述得出结论,,每天1-6g肉桂树皮粉末,对2型糖尿病患者具有降血糖作用80。肉桂在临床和临床前环境中都表现出抗高血压、抗肥胖和降脂的特性,使其可能成为代谢综合征和PCOS治疗的候选药物81,82。
对五项随机对照试验的统计分析发现,肉桂可以改善PCOS女性的胰岛素抵抗83。在其中一项试验中,80名PCOS女性被随机分配接受每天1.5g肉桂粉,分三次服用,或安慰剂治疗12周。肉桂组在空腹胰岛素、胰岛素抵抗和LDL胆固醇方面的下降幅度明显大于安慰剂组84。在一项针对84名患有PCOS和超重或肥胖的受试者(20-38岁)的安慰剂对照试验中,8周内每天1.5g肉桂可提高抗氧化状态,减少氧化应激,改善总胆固醇、LDL和HDL胆固醇水平85。在PCOS的啮齿动物模型中,在雄激素治疗中添加肉桂会减弱单独雄激素治疗时卵巢功能和结构的变化;肉桂的添加也导致了更正常水平的多种性激素86。
12.姜黄素:
姜黄素可减少氧化应激和炎症,并已被证明可改善葡萄糖和脂质代谢以及胰岛素敏感性87。对三项随机对照试验的统计分析发现,每天补充500–1500mg的姜黄素可改善空腹血糖,PCOS患者的胰岛素水平、胰岛素敏感性以及高密度脂蛋白和总胆固醇88。
在荟萃分析中的一项试验中,60名PCOS患者接受了500mg姜黄素或安慰剂治疗,每天两次,为期六周。与安慰剂相比,姜黄素治疗的PCOS女性血清胰岛素显著降低,胰岛素敏感性改善89。在统计分析的另一项试验中,67名PCOS女性接受了500mg姜黄素,每日三次或安慰剂治疗,持续12周。试验结束时,与对照组相比,姜黄素组的空腹血糖和雄激素水平显著下降90。在一项针对72名PCOS患者的对照试验中,每天服用1500mg姜黄素治疗12周,也显示出比安慰剂更能上调PPAR-γ激活分子的表达,改善氧化应激标志物91。
13.白藜芦醇:
白藜芦醇是一种存在于葡萄皮、花生和日本虎杖等抗氧化、抗炎的植物多酚,并在动物研究和临床试验中都证明了其雌激素作用92,93。动物和人类研究的结果表明,白藜芦醇可改善PCOS的代谢参数、雄激素水平、卵巢功能和生育能力94。
在78名多囊卵巢综合征患者的随机安慰剂对照试验中,每天服用1000mg白藜芦醇三个月后,月经规律增加,脱发减少,但其他生殖和代谢指标没有变化95。一项针对30名多囊卵巢综合征(PCOS)女性的随机对照试验发现,连续三个月每天1,500mg白藜芦醇可降低总睾酮、硫酸脱氢表雄酮(DHEA-S)和空腹胰岛素水平;白藜芦醇治疗也增加了胰岛素敏感性96。
在一项随机对照试验中,61名PCOS相关不孕妇女在诱导排卵和取卵进行试管婴儿之前,每天服用800mg白藜芦醇或安慰剂40天。那些接受白藜芦醇治疗的患者有更多高质量的卵母细胞和受精后胚胎。与安慰剂相比,还发现降低了总睾酮和LH水平,增加了FSH水平97。一项针对40名PCOS患者的公开试验发现,每天服用40天800mg白藜芦醇,可以降低炎症细胞因子和CRP水平,以及一种称为内质网应激的细胞应激标志物水平98。内质网应激引起的异常蛋白被认为在PCOS相关的卵巢功能障碍中发挥作用99。
14.褪黑素:
褪黑素是由松果体分泌的一种激素,调节体内的睡眠-觉醒(昼夜节律)周期,并具有清除自由基的作用。在健康个体中,褪黑素水平呈现出每日规律,在晚上达到峰值,在早上下降。褪黑激素受体的遗传变异与PCOS的风险增加有关,睡眠障碍包括睡眠呼吸暂停在PCOS患者中很常见100。
PCOS患者的昼夜节律控制系统似乎失调。在一项包括321名有或没有PCOS症状的女性志愿者的研究中,较高的早晨褪黑激素水平与较多的PCOS相关特征(雄激素过多、少或无月经、卵巢囊性)的表达相关,这表明PCOS可能与昼夜节律信号中断有关。该研究还发现,早晨皮质醇水平过高与PCOS症状数量之间存在关系。由于皮质醇分泌也遵循与褪黑激素大致相反的昼夜节律模式,这一发现进一步证实了PCOS女性可能存在昼夜节律紊乱101。一项针对青春期女孩的横断研究指出,基于褪黑激素分泌不规则的早晨昼夜节律失调与PCOS相关的代谢紊乱之间存在关系102。
一项随机、双盲、安慰剂对照试验对84名PCOS女性进行了研究,发现每天服用6mg褪黑激素和250mg氧化镁,持续8周,与基线相比,减少了不必要的毛发生长、血清胰岛素、总睾酮、总胆固醇和LDL胆固醇,提高了HDL胆固醇和总抗氧化能力103,104。一项针对40名PCOS女性的前瞻性队列研究发现,补充褪黑激素可降低男性激素水平,使其他生殖激素正常化,并改善月经规律105。在一项随机对照试验中,526名患有PCOS相关不孕症的妇女,在肌醇治疗的基础上每天添加3mg褪黑素可改善体外授精(IVF)前后的卵子质量106。
15.亚麻籽和亚麻籽油:
亚麻籽是木脂素(调节雌激素活性的植物化合物)和α-亚麻酸(ω-3脂肪酸)的来源。在动物模型中,亚麻籽油被发现可以调节激素信号传导,改善脂质代谢,并部分通过改变肠道微生物组组成来减少与PCOS相关的炎症107-109。亚麻籽粉也是膳食纤维的来源,这也可能对PCOS有益。
在一项由41名PCOS患者完成的随机、开放标签对照试验中,那些改变生活方式并在12周内每天服用30g亚麻籽粉(约2汤匙)的患者与单独改变生活方式相比,表现出了一些改善。这些变化包括体重、胰岛素抵抗、甘油三酯、hs-CRP、瘦素(一种食欲调节激素,其高水平通常与肥胖有关)、HDL胆固醇和脂联素的改善110。在一份病例报告中,在一名31岁的PCOS患者中,连续四个月每天30g亚麻籽粉与雄激素水平降低和不必要的毛发生长有关109。
更多内容可点击其个性化综合干预方案如下:
- 多囊卵巢防控要略(调节月经排卵)
- 多囊卵巢防控要略(抗多毛症)
- 多囊卵巢防控要略(防胰岛素抵抗)
- 多囊卵巢防控(20-26岁)
- 多囊卵巢防控(27-34岁)
- 多囊卵巢防控(35-42岁)
- 多囊卵巢防控(43岁以上)
注意:需要了解多囊卵巢综合征与生育关系,可点击本网专文:
参阅本网如下专文了解更多相关内容:
医疗干预
治疗需要根据患者是否想要怀孕而不同。治疗的目标,首先是针对伴有PCOS的潜在胰岛素抵抗。
其他治疗措施可包括如下:
- 管理症状
- 减肥,如果超重
- 药物改善胰岛素抵抗,糖耐量和糖尿病前期管理
- 口服避孕药
- 诱导排卵(如果想怀孕)如:
- 二甲双胍或克罗米芬
- 先进的生殖技术
- 预防并发症
- 抗雄激素药物,阻断多毛症
- 激素疗法:避孕药调节月经周期。此外,通过使子宫内膜定期脱落,减少内膜过度生长引起癌变的风险。还可通过抑制雄激素过高,控制异常的毛发生长和痤疮。当PCOS妇女准备怀孕时,可以使用生殖药物来刺激排卵。
预防
没有预防多囊卵巢综合征(PCOS)的指南。参考文献:
1. Sortino MA et al. Polycystic Ovary Syndrome: Insights into the Therapeutic Approach with Inositols. Front Pharmacol. 2017;8:341.
2. Kamenov Z et al. Inositols in PCOS. Molecules. Nov 27 2020;25(23)
3. Monastra G et al. PCOS and Inositols: Controversial Results and Necessary Clarifications. Basic Differences Between D-Chiro and Myo-Inositol. Front Endocrinol (Lausanne). 2021;12:660381.
4. Caputo M et al. Inositols and metabolic disorders: From farm to bedside. Journal of traditional and complementary medicine. May 2020;10(3):252-259.
5. Watkins OC et al. A review of the role of inositols in conditions of insulin dysregulation and in uncomplicated and pathological pregnancy. Crit Rev Food Sci Nutr. Dec 7 2020:1-49.
6. Unfer V et al. Myo-inositol effects in women with PCOS: a meta-analysis of randomized controlled trials. Endocr Connect. Nov 2017;6(8):647-658.
7. Regidor PA et al. Management of women with PCOS using myo-inositol and folic acid. New clinical data and review of the literature. Hormone molecular biology and clinical investigation. Mar 2 2018;34(2)
8. Facchinetti F et al. Short-term effects of metformin and myo-inositol in women with polycystic ovarian syndrome (PCOS): a meta-analysis of randomized clinical trials. Gynecological endocrinology. Mar 2019;35(3):198-206.
9. Agrawal A et al. Comparison of metformin plus myoinositol vs metformin alone in PCOS women undergoing ovulation induction cycles: randomized controlled trial. Gynecological endocrinology. Jun 2019;35(6):511-514.
10. Prabhakar P et al. Impact of myoinositol with metformin and myoinositol alone in infertile PCOS women undergoing ovulation induction cycles - randomized controlled trial. Gynecological endocrinology. Apr 2021;37(4):332-336.
11. Lagana AS et al. Myo-inositol supplementation reduces the amount of gonadotropins and length of ovarian stimulation in women undergoing IVF: a systematic review and meta-analysis of randomized controlled trials. Archives of gynecology and obstetrics. Oct 2018;298(4):675-684.
12. Davinelli S et al. Targeting Metabolic Consequences of Insulin Resistance in Polycystic Ovary Syndrome by D-chiro-inositol and Emerging Nutraceuticals: A Focused Review. J Clin Med. Apr 2 2020;9(4)
13. Gambioli R et al. The use of D-chiro-Inositol in clinical practice. Eur Rev Med Pharmacol Sci. Jan 2021;25(1):438-446.
14. Nordio M et al. The 40:1 myo-inositol/D-chiro-inositol plasma ratio is able to restore ovulation in PCOS patients: comparison with other ratios. Eur Rev Med Pharmacol Sci. Jun 2019;23(12):5512-5521.
15. Benelli E et al. A Combined Therapy with Myo-Inositol and D-Chiro-Inositol Improves Endocrine Parameters and Insulin Resistance in PCOS Young Overweight Women. International journal of endocrinology. 2016;2016:3204083.
16. Le Donne M et al. Effects of three treatment modalities (diet, myoinositol or myoinositol associated with D-chiro-inositol) on clinical and body composition outcomes in women with polycystic ovary syndrome. Eur Rev Med Pharmacol Sci. Mar 2019;23(5):2293-2301.
17. Mendoza N et al. High dose of d-chiro-inositol improves oocyte quality in women with polycystic ovary syndrome undergoing ICSI: a randomized controlled trial. Gynecological endocrinology. May 2020;36(5):398-401.
18. Chandil N et al. Comparison of Metformin and N Acetylcysteine on Clinical, Metabolic Parameter and Hormonal Profile in Women with Polycystic Ovarian Syndrome. J Obstet Gynaecol India. Feb 2019;69(1):77-81.
19. El Sharkwy IA et al. Randomized controlled trial of N-acetylcysteine versus l-carnitine among women with clomiphene-citrate-resistant polycystic ovary syndrome. International journal of gynaecology and obstetrics. Oct 2019;147(1):59-64.
20. Nemati M et al. Comparison of metformin and N-acetyl cysteine, as an adjuvant to clomiphene citrate, in clomiphene-resistant women with polycystic ovary syndrome. J Gynecol Obstet Hum Reprod. Sep 2017;46(7):579-585.
21. Mostajeran F et al. N-Acetylcysteine as an Adjuvant to Letrozole for Induction of Ovulation in Infertile Patients with Polycystic Ovary Syndrome. Advanced biomedical research. 2018;7:100.
22. Behrouzi Lak T et al. N-acetyl cysteine in ovulation induction of PCOS women underwent intrauterine insemination: An RCT. Int J Reprod Biomed. Apr 2017;15(4):203-208.
23. Cheraghi E et al. N-Acetylcysteine Compared to Metformin, Improves The Expression Profile of Growth Differentiation Factor-9 and Receptor Tyrosine Kinase c-Kit in The Oocytes of Patients with Polycystic Ovarian Syndrome. Int J Fertil Steril. Jan 2018;11(4):270-278.
24. Muscogiuri G et al. Shedding new light on female fertility: The role of vitamin D. Rev Endocr Metab Disord. Sep 2017;18(3):273-283.
25. Mu Y. Vitamin D and Polycystic Ovary Syndrome: a Narrative Review. Reprod Sci. Aug 2021;28(8):2110-2117.
26. Kalyanaraman R et al. A Narrative Review of Current Understanding of the Pathophysiology of Polycystic Ovary Syndrome: Focus on Plausible Relevance of Vitamin D. Int J Mol Sci. May 5 2021;22(9)
27. Davis EM et al. Associations between vitamin D levels and polycystic ovary syndrome phenotypes. Minerva endocrinologica. Jun 2019;44(2):176-184.
28. Kumar A et al. Correlation of Vitamin D with metabolic parameters in polycystic ovarian syndrome. J Family Med Prim Care. Jan-Mar 2017;6(1):115-119.
29. Miao CY et al. Effect of vitamin D supplementation on polycystic ovary syndrome: A meta-analysis. Exp Ther Med. Apr 2020;19(4):2641-2649.
30. Jin B et al. Influence of vitamin D supplementation on lipid levels in polycystic ovary syndrome patients: a meta-analysis of randomized controlled trials. J Int Med Res. Aug 2020;48(8):300060520935313.
31. Guo S et al. Vitamin D Supplementation Ameliorates Metabolic Dysfunction in Patients with PCOS: A SystematicReview of RCTs and Insight into the Underlying Mechanism. International journal of endocrinology. 2020;2020:7850816.
32. Al-Bayyari N et al. Androgens and hirsutism score of overweight women with polycystic ovary syndrome improved after vitamin D treatment: A randomized placebo controlled clinical trial. Clin Nutr. Mar 2021;40(3):870-878.
33. Salek M et al. N-3 fatty acids as preventive and therapeutic agents in attenuating PCOS complications. Excli j. 2019;18:558-575.
34. Lu L et al. Dietary and serum omega-3 polyunsaturated fatty acids and PCOS: A matched case-control study. Br J Nutr. 2022 Jul 14;128(1):114-123.
35. Yang K et al. Effectiveness of Omega-3 fatty acid for polycystic ovary syndrome: a systematic review and meta-analysis. Reproductive biology and endocrinology. Mar 27 2018;16(1):27.
36. ScienceDirect. Adiponectin. 12/3/2021. https://www.sciencedirect.com/topics/medicine-and-dentistry/adiponectin
37. Tosatti JAG et al. Influence of n-3 fatty acid supplementation on inflammatory and oxidative stress markers in patients with polycystic ovary syndrome: a systematic review and meta-analysis. Br J Nutr. Mar 28 2021;125(6):657-668.
38. Khani B et al. Omega-3 supplementation effects on polycystic ovary syndrome symptoms and metabolic syndrome. Journal of research in medical sciences. 2017;22:64.
39. Kostov K. Effects of Magnesium Deficiency on Mechanisms of Insulin Resistance in Type 2 Diabetes: Focusing on the Processes of Insulin Secretion and Signaling. Int J Mol Sci. Mar 18 2019;20(6)
40. Babapour M et al. Associations Between Serum Magnesium Concentrations and Polycystic Ovary Syndrome Status: a Systematic Review and Meta-analysis. Biol Trace Elem Res. Apr 2021;199(4):1297-1305.
41. Luo X et al. Associations of Serum Magnesium With Insulin Resistance and Testosterone in Women With Polycystic Ovary Syndrome. Front Endocrinol (Lausanne). 2021;12:683040.
42. Farsinejad-Marj M et al. Clinical and Metabolic Responses to Magnesium Supplementation in Women with Polycystic Ovary Syndrome. Biol Trace Elem Res. Aug 2020;196(2):349-358.
43. Higdon J. Lipoic Acid. Linus Pauling Institute. Updated 1/2019, https://lpi.oregonstate.edu/mic/dietary-factors/lipoic-acid#summary
44. Mahmoudi-Nezhad M et al. An updated systematic review and dose-response meta-analysis of the effects of α-lipoic acid supplementation on glycemic markers in adults. Nutrition. Feb 2021;82:111041.
45. Genazzani AD et al. Modulatory effects of alpha-lipoic acid (ALA) administration on insulin sensitivity in obese PCOS patients. J Endocrinol Invest. May 2018;41(5):583-590.
46. Masharani U et al. Effects of controlled-release alpha lipoic acid in lean, nondiabetic patients with polycystic ovary syndrome. J Diabetes Sci Technol. Mar 1 2010;4(2):359-64.
47. Cirillo F et al. HMGB1 is increased in adolescents with polycystic ovary syndrome (PCOS) and decreases after treatment with myo-inositol (MYO) in combination with alpha-lipoic acid (ALA). Gynecological endocrinology. Jul 2020;36(7):588-593.
48. De Cicco S et al. Myoinositol combined with alpha-lipoic acid may improve the clinical and endocrine features of polycystic ovary syndrome through an insulin-independent action. Gynecological endocrinology. Sep 2017;33(9):698-701.
49. Fruzzetti F et al. Long-term treatment with alpha-lipoic acid and myo-inositol positively affects clinical and metabolic features of polycystic ovary syndrome. Gynecological endocrinology. Feb 2020;36(2):152-155.
50. Fruzzetti F et al. Clinical and Metabolic Effects of Alpha-Lipoic Acid Associated with Two Different Doses of Myo-Inositol in Women with Polycystic Ovary Syndrome. International journal of endocrinology. 2020;2020:2901393.
51. Piotrowska A et al. The Possibilities of Using Chromium Salts as an Agent Supporting Treatment of Polycystic Ovary Syndrome. Biol Trace Elem Res. Dec 2019;192(2):91-97.
52. Zaeemzadeh N et al. Comparison of dietary micronutrient intake in PCOS patients with and without metabolic syndrome. Journal of ovarian research. Jan 9 2021;14(1):10.
53. Ashoush S et al. Chromium picolinate reduces insulin resistance in polycystic ovary syndrome: Randomized controlled trial. J Obstet Gynaecol Res. Mar 2016;42(3):279-85.
54. Lucidi RS et al. Effect of chromium supplementation on insulin resistance and ovarian and menstrual cyclicity in women with polycystic ovary syndrome. Fertility and sterility. Dec 2005;84(6):1755-7.
55. Lydic ML et al. Chromium picolinate improves insulin sensitivity in obese subjects with polycystic ovary syndrome. Fertility and sterility. Jul 2006;86(1):243-6.
56. Fazelian S et al. Chromium supplementation and polycystic ovary syndrome: A systematic review and meta-analysis. Journal of trace elements in medicine and biology : organ of the Society for Minerals and Trace Elements (GMS). Jul 2017;42:92-96.
57. Tang XL et al. Chromium supplementation in women with polycystic ovary syndrome: Systematic review and meta-analysis. J Obstet Gynaecol Res. Jan 2018;44(1):134-143.
58. Bene J et al. Role of carnitine and its derivatives in the development and management of type 2 diabetes. Nutr Diabetes. Mar 7 2018;8(1):8. doi:10.1038/s41387-018-0017-1
59. Savic D et al. The Importance of the Fatty Acid Transporter L-Carnitine in Non-Alcoholic Fatty Liver Disease (NAFLD). Nutrients. Jul 22 2020;12(8)
60. Celik F et al. Plasma L-carnitine levels of obese and non-obese polycystic ovary syndrome patients. J Obstet Gynaecol. May 2017;37(4):476-479.
61. Salehpour S et al. Effects of L-carnitine on Polycystic Ovary Syndrome. JBRA Assist Reprod. Oct 14 2019;23(4):392-395.
62. Ismail AM et al. Adding L-carnitine to clomiphene resistant PCOS women improves the quality of ovulation and the pregnancy rate. A randomized clinical trial. European journal of obstetrics, gynecology, and reproductive biology. Sep 2014;180:148-52.
63. Tauqir S et al. Acetyl-L-Carnitine Ameliorates Metabolic and Endocrine Alterations in Women with PCOS: A Double-Blind Randomized Clinical Trial. Adv Ther. Jul 2021;38(7):3842-3856.
64. He FF et al. Role of gut microbiota in the development of insulin resistance and the mechanism underlying polycystic ovary syndrome: a review. Journal of ovarian research. Jun 17 2020;13(1):73.
65. Li Y et al. Effects of probiotics, prebiotics, and synbiotics on polycystic ovary syndrome: a systematic review and meta-analysis. Crit Rev Food Sci Nutr. Jul 21 2021:1-17.
66. Cozzolino M et al. Therapy with probiotics and synbiotics for polycystic ovarian syndrome: a systematic review and meta-analysis. Eur J Nutr. Oct 2020;59(7):2841-2856.
67. Karimi E et al. The effect of synbiotics supplementation on anthropometric indicators and lipid profiles in women with polycystic ovary syndrome: a randomized controlled trial. Lipids in health and disease. Apr 6 2020;19(1):60.
68. Tillhon M et al. Berberine: new perspectives for old remedies. Biochem Pharmacol. Nov 15 2012;84(10):1260-7.
69. Rondanelli M et al. Berberine Phospholipid Is an Effective Insulin Sensitizer and Improves Metabolic and Hormonal Disorders in Women with Polycystic Ovary Syndrome: A One-Group Pretest-Post-Test Explanatory Study. Nutrients. 2021;13(10):3665.
70. Li MF et al. The Effect of Berberine on Polycystic Ovary Syndrome Patients with Insulin Resistance (PCOS-IR): A Meta-Analysis and Systematic Review. Evid Based Complement Alternat Med. 2018;2018:2532935.
71. Wang Z et al. Berberine improves ovulation and endometrial receptivity in polycystic ovary syndrome. Phytomedicine. Oct 2021;91:153654.
72. Zhang SW et al. Effect and mechanism of berberine against polycystic ovary syndrome. Biomed Pharmacother. Jun 2021;138:111468.
73. Wei W et al. A clinical study on the short-term effect of berberine in comparison to metformin on the metabolic characteristics of women with polycystic ovary syndrome. Eur J Endocrinol. Jan 2012;166(1):99-105.
74. An Y et al. The use of berberine for women with polycystic ovary syndrome undergoing IVF treatment. Clin Endocrinol (Oxf). Mar 2014;80(3):425-31.
75. Yu J et al. Protective effects of berberine in a rat model of polycystic ovary syndrome mediated via the PI3K/AKT pathway. J Obstet Gynaecol Res. May 2021;47(5):1789-1803.
76. Shen HR et al. Berberine exerts a protective effect on rats with polycystic ovary syndrome by inhibiting the inflammatory response and cell apoptosis. Reproductive biology and endocrinology : RB&E. Jan 7 2021;19(1):3.
77. Kysenius K et al. Mitochondria and NMDA receptor-dependent toxicity of berberine sensitizes neurons to glutamate and rotenone injury. PLoS One. 2014;9(9):e107129. doi:10.1371/journal.pone.0107129
78. Mikes V, Dadák V. Berberine derivatives as cationic fluorescent probes for the investigation of the energized state of mitochondria. Biochim Biophys Acta. May 27 1983;723(2):231-9.
79. Mikes V et al. Interaction of fluorescent berberine alkyl derivatives with respiratory chain of rat liver mitochondria. J Bioenerg Biomembr. Feb 1985;17(1):23-32.
80. Santos HO et al. To what extent does cinnamon administration improve the glycemic and lipid profiles? Clin Nutr ESPEN. Oct 2018;27:1-9.
81. Mollazadeh H et al. Cinnamon effects on metabolic syndrome: a review based on its mechanisms. Iranian journal of basic medical sciences. Dec 2016;19(12):1258-1270.
82. Shirzad F et al. Cinnamon effects on blood pressure and metabolic profile: A double-blind, randomized, placebo-controlled trial in patients with stage 1 hypertension. Avicenna journal of phytomedicine. Jan-Feb 2021;11(1):91-100.
83. Heshmati J et al. The effect of cinnamon supplementation on glycemic control in women with polycystic ovary syndrome: A systematic review and meta-analysis. J Food Biochem. Jan 2021;45(1):e13543.
84. Hajimonfarednejad M et al. Insulin resistance improvement by cinnamon powder in polycystic ovary syndrome: A randomized double-blind placebo controlled clinical trial. Phytother Res. Feb 2018;32(2):276-283.
85. Borzoei A et al. Effects of cinnamon supplementation on antioxidant status and serum lipids in women with polycystic ovary syndrome. Journal of traditional and complementary medicine. Jan 2018;8(1):128-133.
86. Dou L et al. The effect of cinnamon on polycystic ovary syndrome in a mouse model. Reproductive biology and endocrinology. Oct 19 2018;16(1):99.
87. Den Hartogh DJ et al. Antidiabetic Properties of Curcumin II: Evidence from In Vivo Studies. Nutrients. Dec 25 2019;12(1)
88. Chien YJ et al. Effects of Curcumin on Glycemic Control and Lipid Profile in Polycystic Ovary Syndrome: Systematic Review with Meta-Analysis and Trial Sequential Analysis. Nutrients. Feb 21 2021;13(2)
89. Sohaei S et al. The effects of curcumin supplementation on glycemic status, lipid profile and hs-CRP levels in overweight/obese women with polycystic ovary syndrome: A randomized, double-blind, placebo-controlled clinical trial. Complement Ther Med. Dec 2019;47:102201.
90. Heshmati J et al. Effects of curcumin supplementation on blood glucose, insulin resistance and androgens in patients with polycystic ovary syndrome: A randomized double-blind placebo-controlled clinical trial. Phytomedicine. Jan 2021;80:153395.
91. Heshmati J et al. The effects of curcumin supplementation on oxidative stress, Sirtuin-1 and peroxisome proliferator activated receptor gamma coactivator 1alpha gene expression in polycystic ovarian syndrome (PCOS) patients: A randomized placebo-controlled clinical trial. Diabetes Metab Syndr. Mar - Apr 2020;14(2):77-82.
92. Cai X et al. Phytoestrogens for the Management of Endometriosis: Findings and Issues. Pharmaceuticals (Basel). Jun 14 2021;14(6)
93. Pasquariello R et al. The Role of Resveratrol in Mammalian Reproduction. Molecules. Oct 5 2020;25(19)
94. Shojaei-Zarghani S et al. Resveratrol and Markers of Polycystic Ovary Syndrome: a Systematic Review of Animal and Clinical Studies. Reprod Sci. 2022 Sep;29(9):2477-2487.
95. Mansour A et al. Effect of resveratrol on menstrual cyclicity, hyperandrogenism and metabolic profile in women with PCOS. Clin Nutr. Jun 2021;40(6):4106-4112.
96. Banaszewska B et al. Effects of Resveratrol on Polycystic Ovary Syndrome: A Double-blind, Randomized, Placebo-controlled Trial. J Clin Endocrinol Metab. Nov 2016;101(11):4322-4328.
97. Bahramrezaie M et al. Effects of resveratrol on VEGF & HIF1 genes expression in granulosa cells in the angiogenesis pathway and laboratory parameters of polycystic ovary syndrome: a triple-blind randomized clinical trial. J Assist Reprod Genet. Aug 2019;36(8):1701-1712.
98. Brenjian S et al. Resveratrol treatment in patients with polycystic ovary syndrome decreased pro-inflammatory and endoplasmic reticulum stress markers. Am J Reprod Immunol. Jan 2020;83(1):e13186.
99. Kunitomi C, Harada M, Kusamoto A, et al. Induction of aryl hydrocarbon receptor in granulosa cells by endoplasmic reticulum stress contributes to pathology of polycystic ovary syndrome. Mol Hum Reprod. Feb 27 2021;27(3)
100. Spinedi E et al. The Polycystic Ovary Syndrome and the Metabolic Syndrome: A Possible Chronobiotic-Cytoprotective Adjuvant Therapy. International journal of endocrinology. 2018;2018:1349868.
101. Lim AJR et al. Phenotypic spectrum of polycystic ovary syndrome and their relationship to the circadian biomarkers, melatonin and cortisol. Endocrinol Diabetes Metab. Jul 2019;2(3):e00047.
102. Simon SL et al. Morning Circadian Misalignment Is Associated With Insulin Resistance in Girls With Obesity and Polycystic Ovarian Syndrome. J Clin Endocrinol Metab. Aug 1 2019;104(8):3525-3534.
103. Alizadeh M et al. Metabolic and hormonal effects of melatonin and/or magnesium supplementation in women with polycystic ovary syndrome: a randomized, double-blind, placebo-controlled trial. Nutr Metab (Lond). Jun 6 2021;18(1):57.
104. Mousavi R et al. Effects of Melatonin and/or Magnesium Supplementation on Biomarkers of Inflammation and Oxidative Stress in Women with Polycystic Ovary Syndrome: a Randomized, Double-Blind, Placebo-Controlled Trial. Biol Trace Elem Res. 2022 Mar;200(3):1010-1019.
105. Tagliaferri V et al. Melatonin Treatment May Be Able to Restore Menstrual Cyclicity in Women With PCOS: A Pilot Study. Reprod Sci. Feb 2018;25(2):269-275.
106. Pacchiarotti A et al. Effect of myo-inositol and melatonin versus myo-inositol, in a randomized controlled trial, for improving in vitro fertilization of patients with polycystic ovarian syndrome. Gynecological endocrinology. 2016;32(1):69-73.
107. Wang T et al. Dietary α-Linolenic Acid-Rich Flaxseed Oil Exerts Beneficial Effects on Polycystic Ovary Syndrome Through Sex Steroid Hormones-Microbiota-Inflammation Axis in Rats. Front Endocrinol (Lausanne). 2020;11:284.
108. Komal F et al. Impact of different omega-3 fatty acid sources on lipid, hormonal, blood glucose, weight gain and histopathological damages profile in PCOS rat model. J Transl Med. Sep 14 2020;18(1):349.
109. Nowak DA et al. The Effect of Flaxseed Supplementation on Hormonal Levels Associated with Polycystic Ovarian Syndrome: A Case Study. Curr Top Nutraceutical Res. 2007;5(4):177-181.
110. Haidari F et al. The effects of flaxseed supplementation on metabolic status in women with polycystic ovary syndrome: a randomized open-labeled controlled clinical trial. Nutr J. Jan 24 2020;19(1):8.
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国国立卫生研究院大众健康网
www.medlineplus.gov
美国多囊卵巢综合征协会
http://www.pcosupport.org
美国妇产科医师大会
http://www.acog.org
加拿大女性健康网
http://www.womenshealthmatters.ca
其他参考文献:详见具体的综合干预方案
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

